血栓性疾病造成長期殘疾和死亡���,并嚴重威脅公眾健康����。大多數溶栓劑����,尤其是蛋白質制劑�,在循環中的半衰期較短,降低了其溶栓效果。因此���,創造一種智能藥物輸送系統���,能將藥物精準輸送到血栓部位���,并在受控條件下釋放�����,對于有效溶栓至關重要。
近日��,西南大學蠶桑紡織與生物質科學學院Bio-road生物醫用材料研發團隊在《Carbohydrate Polymers》上發表題為“Thrombotic microenvironment responsive crosslinking cyclodextrin metal-organic framework nanocarriers for precise targeting and thrombolysis”的研究論文(10.1016/j.carbpol.2024.122058)��。該研究開發了一種獨特的金屬有機框架藥物輸送系統(MCRUA)�����,它對活化血小板具有精準靶向性,并在血栓微環境的刺激下釋放藥物�。

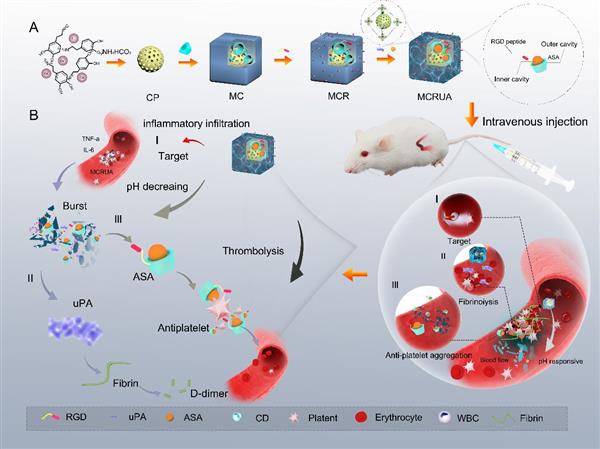
在這項研究工作中�,作者將尿激酶型纖溶酶原激活劑(uPA)和抗炎藥物阿司匹林(乙酰水楊酸��,ASA)加載到具有pH響應性的CaCO3/環糊精交聯金屬有機框架(MC)上����,通過分級功能化技術構建精準靶向血小板的雙重給藥溶栓體系(CaCO3/PDA@CD-MOFs-RGD/uPA/ASA)(MCRUA)��。該體系可智能靶向活化血小板,在血栓部位特殊的病理微環境中解體釋放uPA和ASA,從而改善血栓內的炎癥環境,增強抗血小板聚集效應�����,促進協同溶栓治療��,并能有效防止血管再栓塞的發生��,實現短效溶栓和長效抗凝的作用。