蛋白質(zhì)作為自然界中具有特定功能的復(fù)雜生物大分子,其生物功能的實(shí)現(xiàn)往往依賴于精確的折疊過程。受此啟發(fā),聚合物單鏈納米粒子(SCNP)因其尺寸小、微結(jié)構(gòu)可調(diào)及功能集成等優(yōu)勢,成為模擬蛋白質(zhì)折疊的理想模型。然而,與具有確定多肽序列和長度的蛋白質(zhì)不同,合成聚合物的固有無序性限制了其對復(fù)雜納米結(jié)構(gòu)的精確控制。
近日,課題組提出了一種異質(zhì)光化學(xué)策略。該策略利用光誘導(dǎo)化學(xué)反應(yīng)在空間上的依賴性,成功實(shí)現(xiàn)了聚合物鏈內(nèi)的異質(zhì)聚集和多功能集成。這一方法不僅實(shí)現(xiàn)了單鏈聚合物的折疊,還同步完成了其熒光功能化,為聚合物納米粒子的精確控制和功能化提供了新的思路。

本研究合成了一類新型含氰基苯乙烯(CS)基元的兩親性無規(guī)共聚物。當(dāng)該共聚物在水溶液中進(jìn)行預(yù)折疊時(shí),聚合物鏈中隨機(jī)分布的CS基元表現(xiàn)出獨(dú)特的異質(zhì)聚集行為,具體表現(xiàn)為兩種不同的聚集狀態(tài):緊密聚集態(tài)和單分子分散態(tài)。值得注意的是,處于緊密聚集態(tài)的CS基元能夠發(fā)生光二聚化反應(yīng),從而實(shí)現(xiàn)分子內(nèi)交聯(lián);而單分子分散態(tài)的CS基元?jiǎng)t可通過光環(huán)化反應(yīng)生成具有強(qiáng)綠色熒光的熒光團(tuán)。這種獨(dú)特的雙態(tài)特性使CS基元兼具鏈內(nèi)交聯(lián)劑和熒光功能基團(tuán)的雙重功能,通過雙重光化學(xué)路徑的協(xié)同作用,成功實(shí)現(xiàn)了SCNP的鏈內(nèi)折疊和熒光功能化。
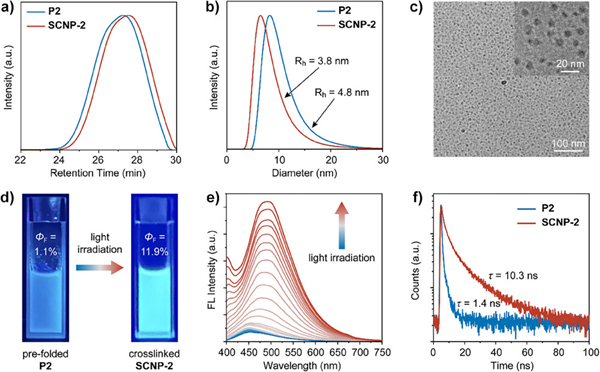
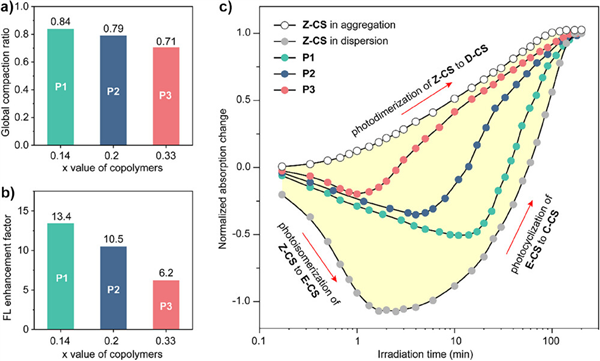
通過調(diào)節(jié)共聚物組成或改變良溶劑比例以控制CS基元的聚集程度,可實(shí)現(xiàn)兩種光化學(xué)反應(yīng)比例的精準(zhǔn)調(diào)控,從而系統(tǒng)性地調(diào)控SCNPs的折疊動(dòng)力學(xué)過程。
此外,通過將尼羅紅染料封裝并結(jié)合鏈內(nèi)能量轉(zhuǎn)移機(jī)制,我們成功實(shí)現(xiàn)了對所得SCNP熒光特性的精細(xì)調(diào)控。這一策略不僅顯著擴(kuò)展了熒光發(fā)射的可調(diào)性范圍,使其能夠產(chǎn)生從綠色到紅色的寬譜發(fā)射,還包括了白光發(fā)射,從而大大增強(qiáng)了該材料在生物成像等領(lǐng)域的應(yīng)用潛力。

本研究成功構(gòu)建了一個(gè)多功能平臺(tái),實(shí)現(xiàn)了SCNPs的同步折疊與功能化。該平臺(tái)有效解決了多個(gè)化學(xué)過程在單鏈體系內(nèi)集成的技術(shù)難題,為復(fù)雜納米結(jié)構(gòu)的精準(zhǔn)設(shè)計(jì)、可控功能化及精確調(diào)控提供了新的解決方案。
相關(guān)研究成果發(fā)表于《Angewandte Chemie International Edition》(Angew. Chem. Int. Ed. 2025, e202500354)。
課題組博士生馬天舒為文章第一作者,田威教授與慕斌副教授為論文共同通訊作者。
論文鏈接:https://doi.org/10.1002/anie.202500354