中科院長(zhǎng)春應(yīng)化所再生醫(yī)學(xué)材料課題組,利用含稀土離子的納米材料成功制備了一種可降解�����、體內(nèi)可MRI示蹤的新型組織工程支架和骨科植入材料����。該研究通過(guò)合成一種GdPO4?H2O納米束,與聚乳酸-聚羥基乙酸共聚物(PLGA)和納米羥基磷灰石(n-HA)復(fù)合,得到的復(fù)合材料支架能夠引導(dǎo)骨骼生成,并能夠利用MRI和CT等臨床常規(guī)影像技術(shù)對(duì)植入材料和新骨生成進(jìn)行實(shí)時(shí)跟蹤觀察���,解決了以往高分子組織工程植入材料不能體內(nèi)示蹤的難題。該研究工作最近發(fā)表于國(guó)際知名雜志Advanced Healthcare
Materials(Advanced
Healthcare Materials, 2016, DOI: 10.1002/adhm.201600249),目前影響因子為5.76����。該研究成果已經(jīng)申請(qǐng)中國(guó)發(fā)明專(zhuān)利(201410522351.9)���。
稀土元素釓(Gd)的化合物及其納米粒子是一種低毒或無(wú)毒T1成像增強(qiáng)劑���,在臨床上已經(jīng)廣泛應(yīng)用的含Gd核磁成像增強(qiáng)劑有如Gd-DTPA(馬根維顯��;磁顯葡胺)、Mn-DPDP(錳福地匹三鈉)等����。課題組針對(duì)骨骼修復(fù)的需要���,合成了一種純六方晶相的磷酸釓(GdPO4?H2O)納米材料�����,其中Gd離子可提供MRI信號(hào),而磷酸根(PO43+)已被認(rèn)為對(duì)骨生長(zhǎng)具有誘導(dǎo)活性。這種長(zhǎng)1微米,直徑30 nm納米棒排列組成的GdPO4?H2O納米束���,在與PLGA/n-HA骨修復(fù)材料復(fù)合后�,在體內(nèi)可產(chǎn)生有效的MRI信號(hào),用于示蹤觀察植入物的動(dòng)態(tài)變化過(guò)程����。同時(shí)��,隨著材料降解和新骨生成,其CT信號(hào)逐漸由弱變強(qiáng)���。通過(guò)MRI和CT的雙示蹤,既可監(jiān)視植入支架的變化過(guò)程�,又可監(jiān)測(cè)到新骨的形成過(guò)程����,這一新技術(shù)為組織工程植入材料的臨床術(shù)后診斷提供有效手段�。GdPO4?H2O納米材料的引入,彌補(bǔ)了高分子可降解組織工程支架體內(nèi)不可示蹤的難題����。經(jīng)過(guò)生物學(xué)檢測(cè)和評(píng)估�,發(fā)現(xiàn)摻入GdPO4?H2O的復(fù)合材料具有較好的生物相容性�,還可明顯促進(jìn)骨鈣素(OCN)的分泌�����,有利于鈣沉積和骨礦化作用���。
在取得上述研究成果的基礎(chǔ)上�����,該課題組正在進(jìn)一步深入研究此項(xiàng)技術(shù)的臨床應(yīng)用可行性。
全文詳見(jiàn): http://onlinelibrary.wiley.com/doi/10.1002/adhm.201600249/full

Scheme 1. Schematic illustration of GdPO4·H2O and GdPO4 nanobundles synthesis and their application in biodegradable bone implants for MR and CT tracing.

Figure 1E.Morphologic analysis of GdPO4·H2O (a–d) and GdPO4 (e–h) nanobundles with SEM (a and e), TEM (b and f), HRTEM (c and g), and SAED (d and h) images
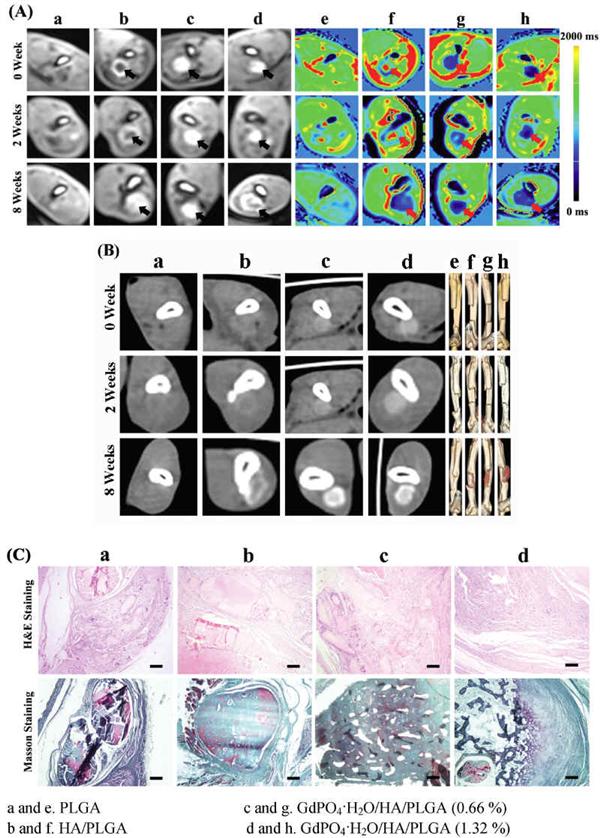
Figure 4. A) T1 MRI images (a–d) and their parametric mapping (e–h) of rabbit radius defects implanted with different materials for 0, 2, and 8 weeks.B) X-ray CT images (a–d) and 3D reconstruction CT images (e–h) of rabbit radius defects implanted with different materials for 0, 2, and 8 weeks.C) H&E and Masson trichrome staining of cross sections of rabbit radius defects implanted for 8 weeks. Bar = 200 μm.