2015年超分子聚合物與大分子自組裝課題組在超分子聚合物自組裝體形貌調(diào)控與藥物控釋研究�、基于超分子交替聚合物的分級(jí)材料制備等方面取得了階段性的成果����。具體體現(xiàn)在以下幾個(gè)方面:
1. 超分子聚合物自組裝體形貌調(diào)控與藥物控釋研究
(1) 課題組利用β-環(huán)糊精和偶氮苯的主客體包合作用�����、以及原子轉(zhuǎn)移自由基聚合法構(gòu)筑了具有支化拓?fù)浣Y(jié)構(gòu)的超分子共聚物。在紫外光-可見光的交替作用下����,此聚合物在水溶液中的自組裝形貌可實(shí)現(xiàn)從空心囊泡到實(shí)心膠束的可逆轉(zhuǎn)化�,此過程中伴隨著超分子聚合物的解離與重構(gòu)。課題組進(jìn)一步利用以上可逆的自組裝形貌轉(zhuǎn)化特性實(shí)現(xiàn)了對(duì)抗癌藥物阿霉素的“開-關(guān)”控釋 (Chem.Commun., 2015, 51, 15366-15369��;被選作內(nèi)封底展示論文)���。以上研究結(jié)果為超分子支化聚合物作為藥物載體在生物醫(yī)學(xué)領(lǐng)域的應(yīng)用提供了可能性����。

圖1 利用超分子支化聚合物自組裝體形貌轉(zhuǎn)化特性實(shí)現(xiàn)藥物分子的“開-關(guān)”控釋
(2) 在此基礎(chǔ)上,課題組進(jìn)一步利用光控的β-環(huán)糊精/偶氮苯的超分子主客體作用�,發(fā)展了一種簡(jiǎn)單��、環(huán)境友好、且高效的聚合物中空納米球的制備方法�。用該方法所制備的中空納米球具有“呼吸”特性�,即:在受到外界刺激時(shí)(如溫度�、pH),納米球的體積會(huì)發(fā)生膨脹或收縮�����。利用這種“呼吸”特性可實(shí)現(xiàn)對(duì)抗癌藥物阿霉素的控制釋放����。細(xì)胞毒性實(shí)驗(yàn)進(jìn)一步證明了該中空納米球具有良好的生物相容性并且是一種具有應(yīng)用前景的阿霉素載體材料(J.
Mater. Chem. B,2015, 3, 8528-8536)。
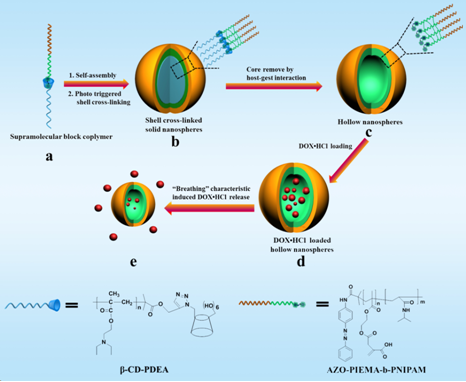
圖2 具有“呼吸”特性的聚合物中空納米球的制備及其藥物控釋研究
(3)課題組針對(duì)目前癌癥治療中存在的多藥耐藥性問題�,通過超分子自組裝原理制備了兩親性接枝共聚物膠束��,并利用其溫度和pH雙重響應(yīng)性實(shí)現(xiàn)了對(duì)膠束表面電荷翻轉(zhuǎn)特性的調(diào)控。這種載藥納米膠束對(duì)抗癌藥物阿霉素具有緩釋作用��,還可以借助靜電作用誘導(dǎo)的內(nèi)吞機(jī)制提高納米膠束的入胞效率��。此外�,MTT實(shí)驗(yàn)表明載藥納米膠束在pH=6.8����、37oC條件下對(duì)耐藥卵巢癌細(xì)胞的抑制生長(zhǎng)效果最好(J. Mater. Chem. B, 2015, 3, 4585-4596)�����。

圖3 利用具有溫度和pH雙重響應(yīng)性的兩親性接枝共聚物膠束的表面電荷翻轉(zhuǎn)特性解決癌癥治療過程中的多藥耐藥性問題
2. 基于超分子交替聚合物的分級(jí)材料的制備
超分子分級(jí)材料在生物醫(yī)藥��、能源環(huán)保等領(lǐng)域具有廣泛的應(yīng)用前景,但目前用一種聚合物體系同時(shí)制備從零維到三維的多維分級(jí)材料仍存在諸多挑戰(zhàn)�。課題組首先利用冠醚和柱[5]芳烴雙重超分子識(shí)別作用合成出了新型的超分子交替聚合物��,其次將其進(jìn)一步制備成零維膠束、一維納米纖維�、二維多孔膜��、三維凝膠等分級(jí)結(jié)構(gòu)材料。此工作為擴(kuò)展超分子聚合物在分級(jí)材料領(lǐng)域的應(yīng)用提供了新途徑(Chem. Eur. J. 2016, 22, 101-105)����。
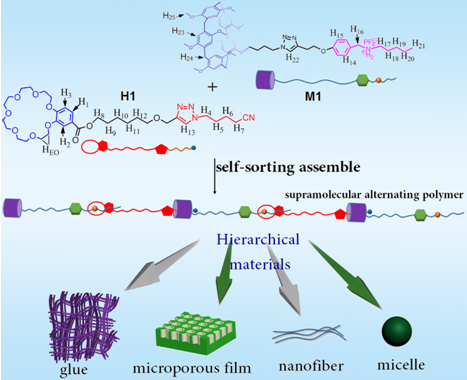
圖4 超分子交替聚合物的合成及其分級(jí)材料的制備