ˮ���z��һ����Hˮ�ۺ���朽��M�ɵľ������S�W�j�ĸߺ�ˮ�ʵ�ܛ���ϣ��V�������ڽM�����̡�ˎ����f��ܛ�w��Ӻ������ȱ����I��Ȼ�������ڹ��r�I�����Ă��y�ۺ���ˮ���z������o��ġ�����ͬ�ԵăȲ��Y������Cе�������ޣ�~ 1 MPa�����������װl�����Ô��ѡ����֮�£�����ܛ�M�����缡�⡢ܛ�ǡ����졢�g���������������z����Ȼˮ���z���M�ɵģ����^���L���M�����������z���и߶�����ķּ��Y���̓��������W���ܣ������쏊�Ȟ�10 MPa����Ȼ�������ɷּ�����ļ{���w�S�����ɵģ���
�ھۺ���ˮ���z�W�j������o�C�{�ײ����������������Ը��������W���ܡ�Ȼ�����ЙC-�o�C֮�g������x�������o�C������Ԫ�ľۼ��͟o��ֲ���ͬ�r���o�C������Ԫ�c�ЙC���|֮�gȱ����ֵĽY�ϣ��@��ʹ���ЙC-�o�C�ͺ�ˮ���z�ęCе���ܵ������ܵ��O������ơ�����Ό��o�C�����ྫ�_�������ЙC�ۺ���������Ȼ��һ����������ܵ���Ȼ����Y���c���ܵĆ��l�����Ƃ��ЙC-�o�C�ͺ�ˮ���z�����^���У����F�ЙC���c�o�C���ځ��{�׳߶�������Y�ϣ��������Ƃ��������������Ȼ�Y���������ܵĸ����Cе���ϡ�
�����n�}�Mǰ�������ßo�C�x�ӹѾ��w��������Y����Nature 2019, 574, 394-398, Angew. Chem. Int. Ed. 2020, 59, 2071-2075���ͷּ�����Y����Adv. Funct. Mater. 2020, 30, 1908556, ACS Appl. Mater. Interfaces 2020, 12, 36731-36739�����ϵľݣ��@�����������һ�N�����o�C�ۺϲ��ԣ���ͨ�^�T���o�C�x�ӹѾ��w�ھۺ��������γɵľW�j�Ͼۺϣ������Ƃ伡�����ЙC-�o�C�ͺ�ˮ���z���ڮ���ۺ��^���У��ЙC�c�o�C���ځ��{�׳߶��ό��F�o�ܽY�ϣ����^�Mһ�������T���ĽY��ȡ���γɸ߶ȷּ�������ЙC-�o�C�{���ɽY�����@�N�Y��ʹ�����Ƃ��ˮ���z���иߏ����g�����W���ܣ����Ȟ�17.84 MPa�������ܞ�8.97 kJ m-2�������^����Ȼ����ͽ^������ϳ�ˮ���z�����⣬�ܓp��ˮ���z����ͨ�^�o�C�x�ӹѾ��w��ԭλ�پۺό��F�ܺõ��ޏ͡�������������ЙC-�o�C���ɽY����ԓ�ͺ�ˮ���z����ͨ�^���̳ɞ�̼�푑��������棬��ˮ�h���б��F���������\�ӡ����о�������ͨ�^�o�C�x�ӹѾ��w�c�ЙC�߷����M�Ю����o�C�ۺϿ��Ԍ��F�����ЙC-�o�C���ɽY���Ę����������ǂ��y���ЙC-�o�C�ͺϣ��@�����M�Y��/���ܲ��ϵ��OӋ�������ṩ��һ�Nȫ�µIJ��ԡ�
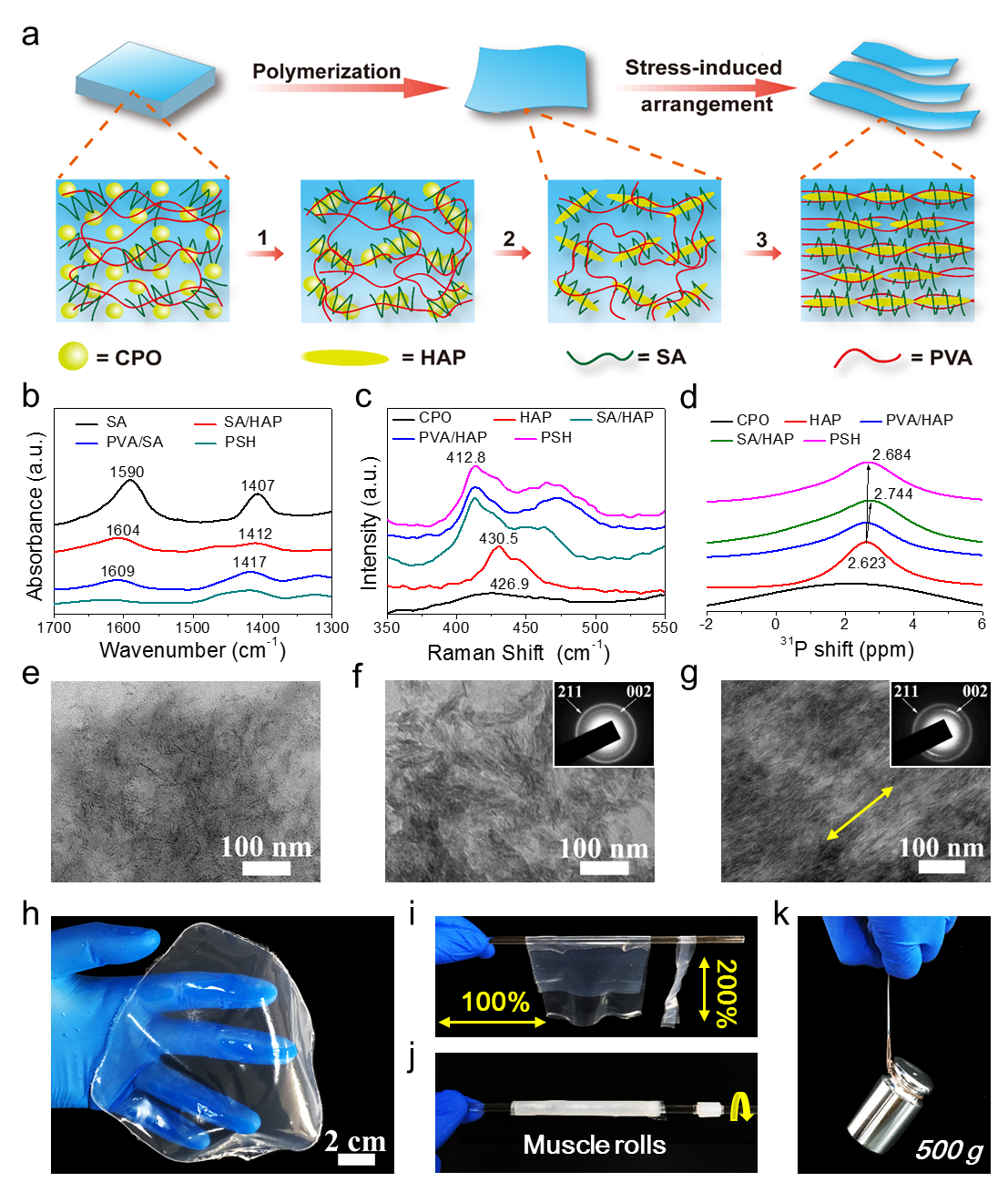
ͨ�^�����o�C�ۺϲ����Ƃ��������ďͺ�ˮ���z����Ȳ��Y��
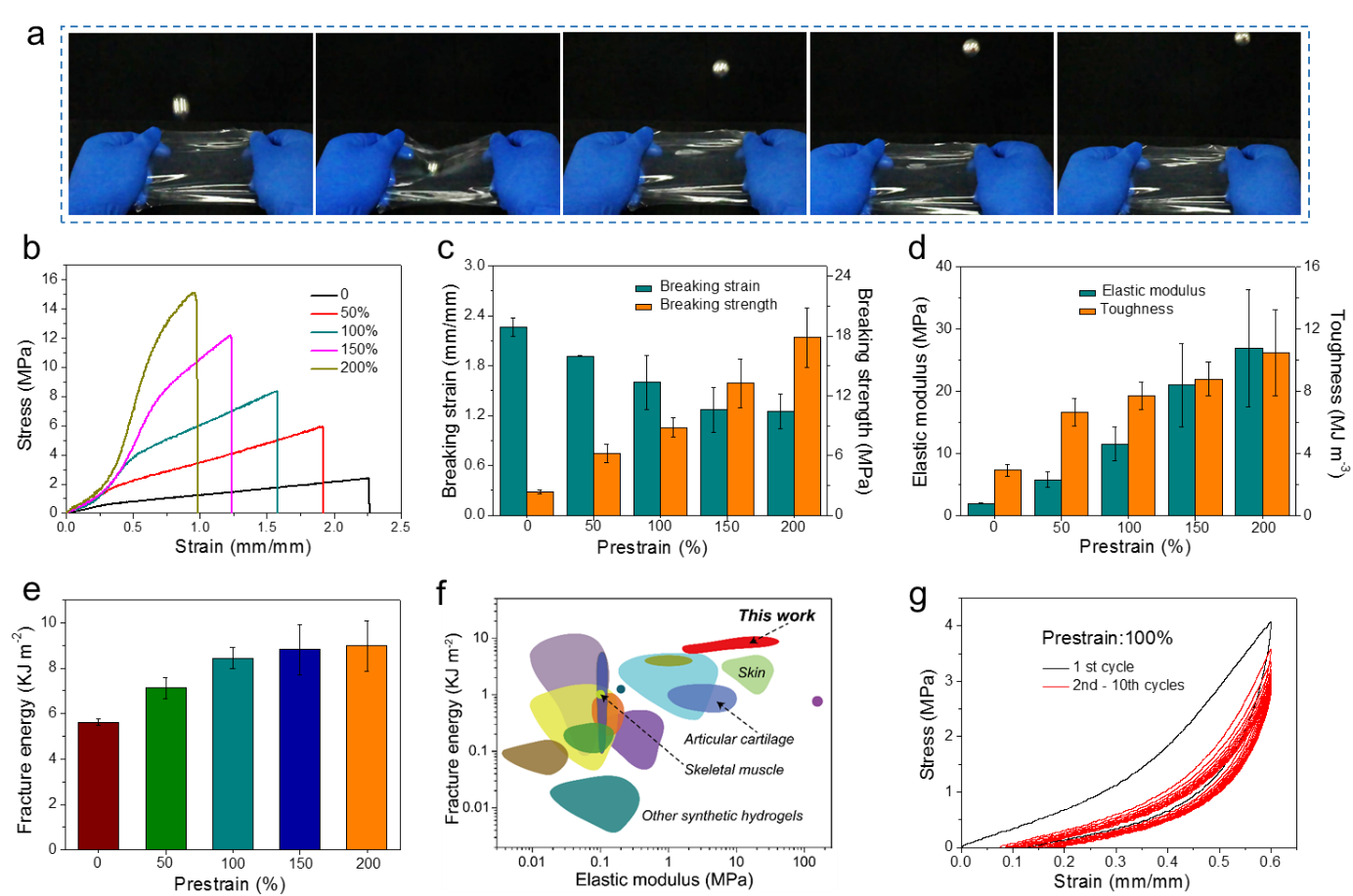
��������ͺ�ˮ���z�ęCе����

��������ͺ�ˮ���zͨ�^ԭλ�ۺϵ��ޏ�����

��������ͺ�ˮ���z��ˮ������
�о��ɹ��l���ڽ��ڵ�ACS Applied Materials & Interfaces�ڿ��ϡ�Փ�ĵĵ�һ���ߞ��㽭��W���Wϵ��ʿ�������|����ͬͨӍ�������㽭��W���Wϵ��������Ƹ���о��T�����������
ԭ��朽ӣ�https://pubs.acs.org/doi/10.1021/acsami.0c18242
- ��ƴ���/�����F� Small����Ȼ�z���cˮ���z��ȡ�����ˡ���������������ˮ���z 2024-02-02
- �͵���W���ۄٽ��ڡ��Oѩ÷�����ڈF����w�S������ӌW�I��ȡ�����Mչ 2019-10-30
- ���ݴ�W�Ε���/������ Adv. Mater.�������ӏͺ�ˮ���z�i����x������\�x��늳�ѭ�h���� 2025-04-21
- �㽭ʡ�����tԺ�O�D�Fꠡ����ݴ�W���M���ڈFꠡ�ACS Nano��������CAT�{��ø��Ĺ������ͺ�ˮ���z���ڼ��{�ع����� 2025-04-12
- �Ĵ���W�����Fꠡ�ACS Nano������ܼ{�����ﮐ�|�Y�ͺ�ˮ���z���� - ���ڂ��ڼ�������Ĥ��Ⱦ���\��һ�w���²��� 2025-03-15
