��ԭ��ʼ����ij��죨�R�e����T���������ֳ������Լ�T�������ߑ���Ч�������ί����[������������P�I�A�Ρ��������������@���N�^���аl(f��)�]�O����Ҫ�����á��C�w����Ȼ�粡ԭ�w��Ⱦ���܉������ҵ����ߑ�����ˡ��²�ԭ�w�������ڼ������߿��[���о������ṩһ�N���H���е��о����ԡ�
�ܴˆ��l(f��)���K�ݴ�Wܛ���ۑB(t��i)�����������о����ď��l(w��i)�|�����ڵ���ǰ���о��аl(f��)�F(xi��n)��Ȼ�Ͼ��Ǹ��Ե�CpG����С��E.G7�[������ģ���ͨ�^���l(f��)��������ϵ�y(t��ng)��ѪҺ������֮һ��T���������[����ԭ�خ���CD8+T������50%��С�������ȫ�����[�����D1, Bioconjugate Chem. 2017, 28, 1993����

�D1 ����������Ч���� abd�����߽ӷN��С���w��(n��i)�خ���CD8+T��������ֳ��r��c��E.G7�[��ģ�͵�����������e���ӷN70���ӛ����CD8+T�����ı�����
δ����Ŀ�ԭ��ʼ��������ͻ����;��ɼ����������ж�Nģʽ�R�e���w����CLR��TLR������ǰ�ڹ������A�ϣ����о������Y��ԓ�о��F��_�l(f��)�Ĺ��T��RAFT�ۺϣ�ACS Macro Letters. 2016, 5, 1278���Ͷ�Ͱ����W���Mһ���l(f��)չһ�N�Gɫ�ϳɡ��²�ԭ�w������IJ��ԣ������ù��T��RAFT�ۺό��������ӻ��F�������ԣ��ɿ��OӋ�ϳ��˺����������Ӻ��ǻ��F�Ĺ���������������ӻ��F�������߷������Ե����c��ԭλ�Ƃ��ǰ����Ľ�{�����ӣ�ͬ�r���������ܻ���������ż(li��n)����{�����ӣ��ɿ��OӋ�ϳ��˺���glucose��CpG������@Au�{�����ӡ��w��RAW-blue��������������@Au�{����������Σ�U��̖��������Ļ��ԡ�
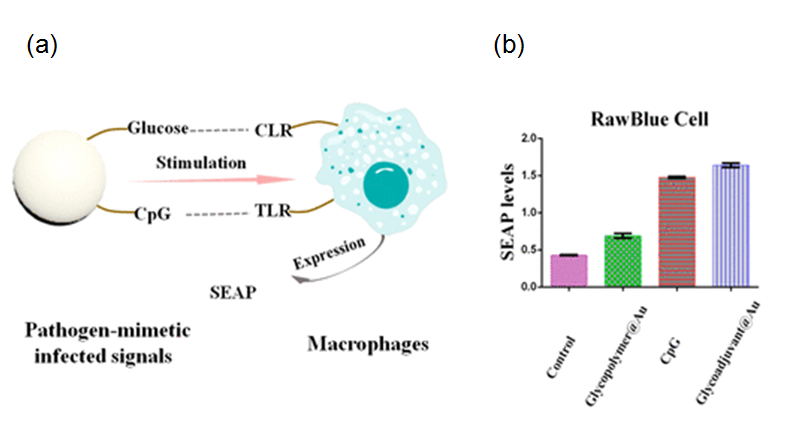
�D2 ����������Ч���� a�������̼���ԭ��ʼ���ʾ��D��b���̼���Raw-blue����SEAP���_��r��
���P�����Ѱl(f��)����ACS Macro Letters. 2018, 7, 70�ϡ�Փ�ĵĵ�һ���ߞ��K�ݴ�W�Tʿ����������ͬͨӍ���ߞ��K�ݴ�Wꐸ߽������c�K�ݴ�W���l(w��i)�|�����ڡ�
Փ��朽ӣ�http://pubs.acs.org/doi/full/10.1021/acsmacrolett.7b00837
- �K���־�h/�������K��һԺ����� Nat. Commun.���[��Ѫ���m���ԡ�ճ���ԺͿ������������ڿɳ��m(x��)�Ľ�(j��ng)���}���W˨���ί� 2025-07-09
- ���ݴ�W�����ƽ��ڈFꠡ�Acta Biomater.����ˎ����;ۺ���{���z�������[���LЧ�ί����о��ɹ� 2025-07-08
- ��ɽ��W�Ƕ�ؔ/�S�ſ�/������/���x�F� Adv. Mater.�������L�v���ԵĿ�ע����̿�{��øˮ���z���F(xi��n)�[���ąf(xi��)ͬ�ί� 2025-07-04
- �|�A��W������/ʷ��ꖈF� Bioact. Mater.�����ڼ{�����z���ί��ͼ{������ͨ�^ȫ���������{(di��o)��(ji��)���F(xi��n)�[�����A����ֱ���ί� 2024-09-25
- �L������ꐌW˼/���fͨ�о��T�F� Nano Lett.���ۇf���������d�w�������Ŀ�ԭ����Ч�� 2024-08-30
- ���A��W�ž��/܊���t(y��)�W�о�Ժ����¡�����F� ACS Nano��һ�N����ɗl��Ȼ����;���ğo�{������ 2024-03-19
