�Y�˲���Tuberculosis��TB�����ɽY�˷�֦�U����Mycobacterium tuberculosis��M.tb����Ⱦ���l(f��)�����Ԃ�Ⱦ�Լ������džβ�ԭ�w�����˔�(sh��)���Ă�Ⱦ�������ڰ��̲������������{�������TB���߿ȳ���M.tb����������������ȱ����ݾ��ɼ������ɲ���M.tb�\�͵���νM��������Ⱦ�ķ��ݾ��ɼ�������ļ�������������_��Ⱦ��λ���γɽY�˽Y��(ji��)��Granuloma�����Y�˽Y��(ji��)��TB�����ԽY�����ɴ������ɼ����o�����ж��ɣ������Ğ顰��������^(q��)������(n��i)������M.tb���c֮�����������ľ��ɼ�����Ƭ���Y�˽Y��(ji��)�����ܽY���܉���Ч���xM.tb��ֹ��Ⱦ�Uɢ�����ǣ������w�������½��r���Y�˽Y��(ji��)��(n��i)��M.tb�����������ֳ�����l(f��)����ԽY�ˡ�����Ҫ���ǣ��Y�˽Y��(ji��)�����ܽY�����������˿������M�룬��ʹ�R���ϳ�Ҏ(gu��)�Ķ�ˎ(li��n)���ί�������Ч������L���������ôĶ����»��������Բ�Y�˲����w�Ӳ�������ˣ���������Y�˽Y��(ji��)���\��ϵ�y(t��ng)�����˷����y(t��ng)�����د�����ȱ�ݣ��ɞ�Y�˲��������\��������
��ɽ��W���ٵ����t(y��)Ժ�����x���S�ء��������ڈF�(li��n)����ۿƼ���W�Ʊ���Ժʿ���w����ʿ���_�l(f��)�˼����;ۼ��l(f��)�⣨AIE�����ϡ����Y��һ��ˎ������ƽ��RIF�����p�H���z�����ӣ�DSPE-PEG2000����һ�w�Ķ�ܼ{���z�����˼{���z�������PEG��܉����L�w��(n��i)�Lѭ�h(hu��n)��AIE���ϰl(f��)�䏊�ҟɹ⌍�F(xi��n)�Y�˽Y��(ji��)���w��(n��i)�����ۙ��AIE�����ڼ��l(f��)�������®a(ch��n)������ROS���F(xi��n)�Y�˾��Ĺ�����������{���z��������RIF���F(xi��n)�Y�˲��İ���f(xi��)ͬ��������K���F(xi��n)�Y�˲��ľ����\�����D1��

�D1. �Y�˲������\��ԭ��D��Step 1��bottom-up�����ϳɶ�ܼ{���z��TTD+RIF NPs��Step 2��TTD+RIF NPsͨ�^�Lѭ�h(hu��n)��EPRЧ�����F(xi��n)�Y�˽Y��(ji��)��������ۙ��Step 3��TTD+RIF NPs���F(xi��n)�Y�˾��Ĺ���������ϲ�ˎ���ί���
ԓ�F�����ϵ�y(t��ng)�ϳ�������AIE����TTD���D2A�����l(f��)�F(xi��n)����аl(f��)�䏊�Ҽtɫ�ɹ����ԣ��D2B�����ۼ��l(f��)�����ԣ��D2C���͏��ҵ�ROS�a(ch��n)�����ԡ�ͨ�^bottom-up��ʽ�ϳ�TTD+RIF NPs���Եõ�������~120 nm�����ͼ{���z��TTD+RIF NPs���D2D������NPs���˾߂�TTD�Ļ�������֮�⣨�D2E����߀�����˿��Y��һ��ˎ��RIF���DF�����Ķ����F(xi��n)�Y�˾��ąf(xi��)ͬ������

�D2. ����AIE����TTD�Ͷ�ܼ{���z��TTD+RIF NPs�ĺϳɺͱ�����
�o�}ע��˶�ܼ{���z��TTD+RIF NPs���ɷN�Y��(ji��)����ģ�ͣ��D3���w��(n��i)��TTD+RIF NPs������������PEG��ӱ����ɼ�������������F(xi��n)�w��(n��i)�Lѭ�h(hu��n)��ͨ�^EPRЧ����TTD+RIF NPs����Y��(ji��)�����F(xi��n)�Y��(ji��)�İ�����D4A,4C�������L�ڜ����Y��(ji��)��λ�����F(xi��n)���Y��(ji��)���L�ڰ���ۙ���D4B����

�D3. (A-C) ����֦�U����Ⱦ���°��R�~��(j��ng)�ܽY��(ji��)ģ�͘�����(D-H) ����֦�U����Ⱦ����С��β���Y��(ji��)ģ�͘���

�D4. (A) TTD+RIF NPs���F(xi��n)���R�~�Y��(ji��)�İ������(B) TTD+RIF NPs���F(xi��n)���R�~���Y��(ji��)�İ���ۙ��(A) TTD+RIF NPs���F(xi��n)С��β���Y��(ji��)�������
�����R�~�ֲ��Y��(ji��)�M�й��գ�����چμ�RIF�ί��M��PBS�M��TTD+RIF NPs�܉��@���������R�~�Y��(ji��)��(n��i)���ĺ���֦�U�����D5A,5B�������R�~�����ʴ����ߣ��D5C��������Ҫ���ǣ�TTD+RIF NPs߀�܉��@��������RIF��ȫ��ˎ����ˎ�ԽY�˗U�����D5D,5F�����Aʾ��TTD+RIF NPs���ί��R����ˎ�ԽY�˵ľ������C�ϣ����ھۼ��l(f��)��Ķ�ܼ{���z��TTD+RIF NPs�ļ{���dˎ�wϵ���Ԍ��F(xi��n)���Y�˽Y��(ji��)�İ�������ۙ���܉��@�������Y��(ji��)��(n��i)���IJ�ԭ�������R����ˎ���К���Ч�����錍�F(xi��n)�Y�˲������\���ṩ�µ�˼·�����о���R�����Ý�����
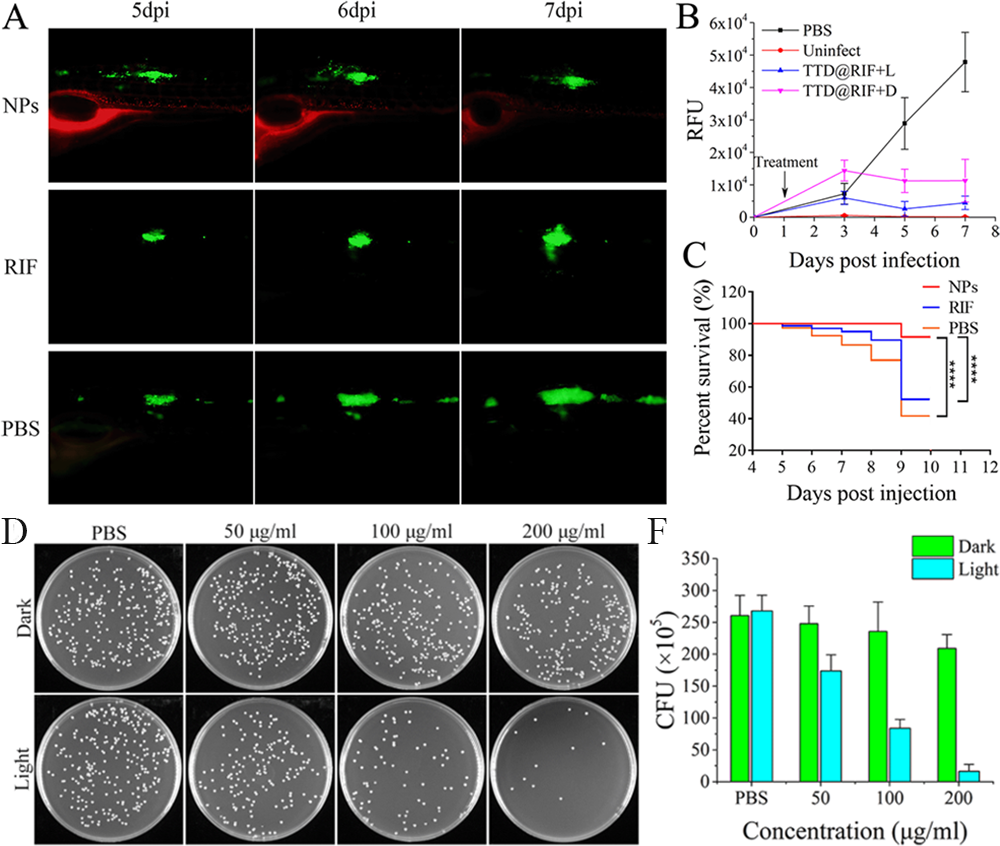
�D5. (A-C) TTD+RIF NPs���F(xi��n)���R�~�Y��(ji��)��λ����֦�U���Ĺ���������ϲ�ˎ���ί���(D-F) TTD+RIF NPs���F(xi��n)��ˎ�Y�˾�����Ч������
Փ����Ϣ��Yuhui Liao?, Bin Li?, Zheng Zhao?, Yu Fu, Qingqin Tan, Xingyu Li, Wei Wang, Jialing Yin, Hong Shan*, Ben Zhong Tang*, Xi Huang*. Targeted Theranostics for Tuberculosis: A Rifampicin-Loaded Aggregation-Induced Emission Carrier for Granulomas-Tracking and Anti-Infection. ACS Nano. 10.1021/acsnano.0c00586 (SCI indexed, IF= 13.903; ���̼��gһ�^(q��))
Փ��朽ӣ�https://doi.org/10.1021/acsnano.0c00586
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ/�w�����ڈFꠡ�ACS Nano��������Ĥ����ľۼ��T���l(f��)�����������(j��ng)ۙ�͓p���Ŀ�ҕ�� 2025-01-21
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ�c�w�����ڈFꠡ�ACS Nano���C�����ۼ��T���l(f��)����ό��F(xi��n)�߷ֱ�������� 2025-01-07
- �������Ʊ���Ժʿ/�������賯 AM������AIE���Լ{�ͺ�ˮ���z�Ŀɴ�������ʽ��Ϣ-���в��� 2024-03-23
- ���u��Wκ�ǎ����O�µ� ACS Nano�C�������ڴ̼�푑��Ծۺ���ļ{���wϵ�ڰ��Y�\���е��о��Mչ 2023-12-06
- �Ĵ���W���Ʊ����ڈF� Biomaterials�������������ݹ��ܵļ{���dˎͿ�� 2023-09-16
- �п�Ժ�����������о��T��ꐿ����о��T�n�}�M�ڰl(f��)չ���ʹ̼�푑��Լ���������Է���ȡ���Mչ 2019-05-28
- ����CNRS����F� PNAS���{��ˎ���f��ϵ�y(t��ng) - �ԽM�b���η��ӳ����Ӽ{���z��ͨ�^�ٳּ��������ݵķ�ʽ����f�Ϳ���ˎ�� 2023-06-07
�\���Pע�߷��ӿƼ�

- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g��Ӗ����...
- �����ϸ��Լ��ӹ����gҪ�I��...
- �Ї������ƌW��36%���١���...
- �P���e�k�������Ї�����Ұl(f��)...