Ѫ���fͬ�ޏ��ǽM�������c�����t�W�I���о����R���ش�����Ѫ���������ޏ͵������M�̘O����s��Ҫ���ڲ�ͬ�A�Σ�ͨ�^�����w�錧�ļ����gͨӍ�����F��Ѫ�܃�Ƥ��������Ԫ�ȼ����Ķ���c���A���خ��{�ء�����������������w�Ĵ������ޏͲ����ܵ��ˏV�����Pע��Ȼ�����F�в������R�����w�����̣��H24~4С�r�����������Լ������خ��Լ����{�ع��ܵ�miRNA����׃���������y���٬F��Ȼ�����^���Џ��s���ӑB���{���M�̣���������������Ѫ���fͬ�ޏͷ���đ��á�
11��21�գ��Ї��ƌWԺ�������M���g�о�Ժ�����t�ò����c��е�о����ĶŌW���о��T�F����ھ����{�������w���������Խ�����Ϸ���ȡ����Ҫ�о��Mչ�����P�ɹ��ԡ�A ferroelectric living interface for fine-tuned exosome secretion toward physiology-mimetic neurovascular remodeling�����}���l����Cell Press������Ş�ڿ�Matter�ϡ�ԓ���Խ�����ϣ�LIFES���Y�Ͼ�ƫ����ϩ-������ϩ��P(VDF-TrFE)�������ܸ߷��ӏͺϲ��ό��c�g���|�ɼ����Ļ���ӣ�ͨ�^�ͺϲ��όӵ��ؓ�����̖���g���|�ɼ������{�أ��������F�������w�ij־ã��s192С�r���������������s8����ጷţ����ҿ���Ѫ�����ޏ͵IJ�ͬ�A���{�������w�е�miRNA��ǰ�ڴ�Ѫ�����ɡ����ڴ�����������ģ�M��ȻѪ�����ޏ��^���е��A���خ��{�����ã��Ķ���Ч���M���wѪ���ąfͬ�ޏͣ������������t�ò����c��е�I�������ش���ǰ����

�D1 ��Ѫ���fͬ�ޏ͵�LIFES�OӋ��LIFES��P(VDF-TrFE)�����ܸ߷��ӏͺϲ����Ӻͻ���ӽM�ɣ����Џͺϲ��Ͽ��ṩ���ڼ����{�ص��ؓ䡢��늺������̖��
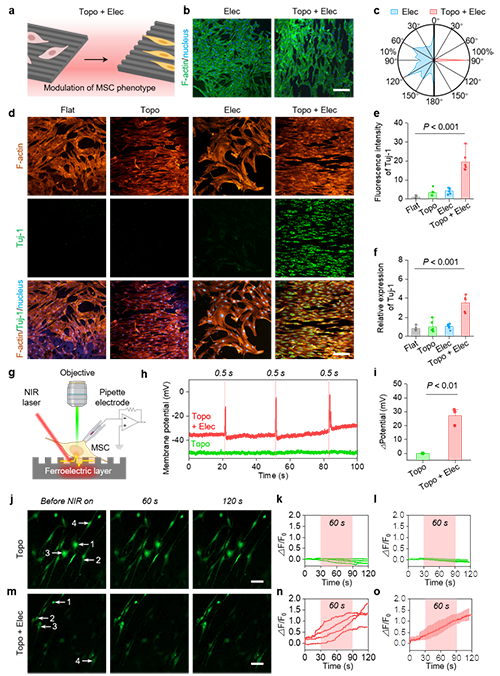
�D2 LIFES�ďͺϲ��όӌ��g���|�ɼ������{������a-c���ͺϲ��όӵ�ȡ��Y�������g���|�����������С���d-f���ؓ���̖�fͬ�����̖���M�g���|�ɼ����ӷֻ�����g-o���������̖���l�g���|�ɼ����������푑������l�}�x�Ӄ�����

�D3 LIFES�����w�����ľ����{�ء���a-c����һ�A�Σ�0~5�죩���M�������ʹ�Ѫ������miRNA�����w�����ڡ���d-f����һ�A�Σ�6~8�죩���M������������miRNA�����w�����ڡ���g��LIFES��ģ�M�����^���������w����c���A���خ�����Ȼ�{�����á�

�D4 LIFES�����w���ھ����{�صęC������a-d����һ�A����0~5�죩���ؓ�͉����̖����MAPK/ERK��PI3K/AKT��̖ͨ·����e-f���ڶ��A����6~8�죩���������̖�����}�x����̖ͨ·�c�ض�푑����P��̖ͨ·��

�D5 LIFES��Ѫ�����ޏ͵��w���u�r����a-f�����MѪ����Ƥ�����w�Ƽ�ë��Ѫ�ܘӾW�j�γ�����g-l�����M�����L�����g�B�ӡ�

�D6 LIFES����������Ѫ�����fͬ�ޏ͡���a-c�����������ڵğo�̺����ϡ���d-f�����M�����ڵ�Ѫ���fͬ�ޏ͡���g-h������ë�Һ����w�ȹ�����Ƥ�w���ٽY����������
�Ї��ƌWԺ�������M���g�о�Ժ�����t�ò����c��е�о������ŌW���о��T��ԓՓ�ĵ�ͨӍ���ߣ���ʿ�о������������w�������о��T�鹲ͬ��һ���ߣ�����������W���������WԺ��������ڡ���ƽ��ʿ�Լ���۴�W�Cе����ϵ�������ڞ�ԓՓ�Ĺ�ͬ���ߣ����о��нo���˴���������
�F��L����Ƹ��ʿ�gӭ�����v�l������xm.du@siat.ac.cn
�Wվ��https://ibmd.siat.ac.cn/
ԭ��朽ӣ�https://pan.baidu.com/s/1EI2A9Hq400q45OmX8kBl1w?pwd=726n
- �п�Ժ�{����Դ��������&�����ֈFꠡ�Chem. Eng. J.���������ЙC-�o�Cͬ�S�Y�������ԉ�늼{���w�S�����Թ���������� 2022-09-16
- �п�Ժ�������MԺ�ŌW���о��T�F� NSR����ء�Һ�ΙC���ˡ� 2022-08-25
- �п�Ժ�������MԺ�ŌW��/�۳Ǵ����@�_��Sci. Adv.�������T����늝������� 2022-07-09
- ���_���������n�}�M����2026����W����Tʿ��ֱ������ - ���όW�����W���߷��ӡ�����W�������c�w�S��Ӌ��ģ�M�������Ϣ... 2025-06-13
- ���_��W���������n�}�M���ղ�ʿ����2025����W�������Y��ʿ��� - ���όW�����W���߷��ӡ�����������W�������c�w�S�����١�Ӌ��ģ�M�������Ϣ�� 2025-04-17
- �Ϻ����M��F� JACS�����ܸ߷���ǰˎͿ�Ӽ��� 2023-11-26
- �|�ϴ�W���������ڈF� JCR: �_�l�d�g���|�ɼ�������ģ�K���ڸ���ȱ�p���ޏ� 2025-04-03
