��Ѫ�ܼ�������ȫ����Ҫ����������s85%������Դ��Ѫ���������µ�ȱѪ�����K�����ڹڠ���}�����ί��I��ˎ��Ϳ�����ң�DCB���������oֲ�����������I�R�����£����g���ǻ�٪Mխ�����_�R��������Ć��}���ڃ�Ƥ���������Ե��Ɖ�--���ҔU�����l��������ROS�����l������Ƥ�����g�o���B�ӣ�TJs���Y�����⣬�M���|�l�װY�L���cƽ�����������������y�����۽�����ֳ��ك�Ƥ������������ҕ��TJs�ޏ��@һ�SϵѪ�ܷ��B������һ����������
��ˣ��㽭��W������/�S�G/�w�o�Fꠣ��Ľ��넓�����l��Ѫ���h��׃�����l�������Ե�������Ƥ���Ͼ����ޏ����������������е�OӋ���_�l��һ�N�ɇ�Ϳ��ROS푑���ˮ���zͿ�ӣ�OA@G-NO/B-EC������������֪��������푑��h��׃���������ޏ̓�Ƥ���ϣ��ƽ��٪Mխ�y�}�����zͿ���m�䳬��Ϳ��ˇ���Ƃ侫�_�ɿأ�������Ҫ���D��������

�о��ɹ�����Sprayable Reactive Oxygen Species-Responsive Hydrogel Coatings Restore Endothelial Barrier Integrity for Functional Vascular Healing�����}�l����ACS Nano�ڿ������õ��㽭��WӋ�������c�οƷ���ڵ�ָ���c֧�֡�

�D1 ROS푑�ˮ���zͿ�ӣ�OA@G-NO/B-EC���ӑB�ޏ̓�Ƥ���ϣ�����Ѫ���٪Mխ�������A�Σ����ғp������TJs�Ɖģ�ROS���l�T�lM1�;��ɼ���������ƽ�����������ޏ��A�Σ�Ϳ�Ӱ���ጷſ������������ROS���ޏ�TJs���cNO�������Ƥ�w�ƣ������DM1/M2���ɼ����O�����ؽ�Ѫ�ܷ��B
������Ҫ�c��
һ��ROS����cNOጷ�ˮ���zͿ��
OA@G-NO/B-ECˮ���zͨ�^���o늇�Ϳ��ˇ���_�Ƃ䣬��Ҫ�ɿ���ı����ῧ������ǰˎ��B-EC���ʹ����һ��������NO�����w��G-NO���M�ɡ�����ͨ�^ϯ��A�����c��Ͱ�����������ǣ�OA���ڹ���Ϳ�^���Ќ��F˲�r�Խ���ˮ���z�܉�ͨ�^���I����x��-���ȶ����������cѪ�܃ȱڰl������á��p�ӑB���r�I��ϯ��A�I+���������I��ʹ��ԓˮ���zͿ������ROS�e�ەr��ۣ�����ጷſ�����������������NO���w�����Y���@ʾ����1 mM H?O?�̼��£�ˎ��ጷ����_��42%��ROS����ʳ��^85%����300 ��M H?O?�̼��£�G-NOጷ������_��60%��
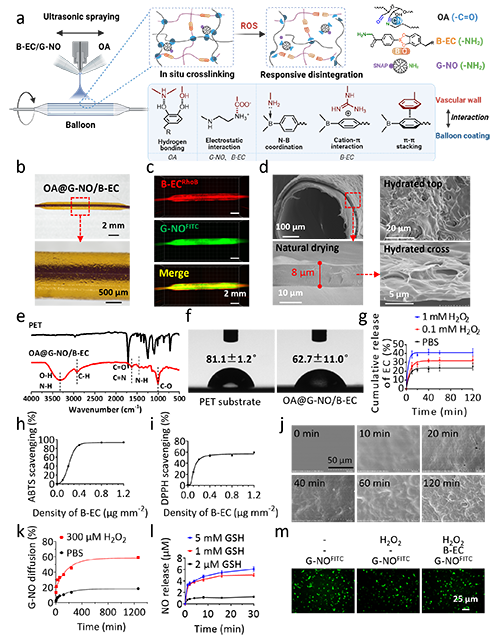
�D2 OA@G-NO/B-EC���zͿ�ӵ��Ƃ��c����
�����ӏ���Ƥ�o���B�ӡ��p�����Լ�������
Ϳ���܉���Ч�֏̓�Ƥ�����gTJs�P�I���ף���ZO-1��Claudin-5��JAM-A�ı��_�քe����26%��111%��54%�����p�پ��ɼ�����𤸽�c�w�ƣ��քe����78%��19%�������̓�Ƥͨ�ԣ�Evan blue��FITC-dextran�ĝB�քe�p��64%��7%����RNA�y�����������Ϳ��ͨ�^���{TJs���P��������NF-��Bͨ·�����M��Ƥ�ޏ͡�
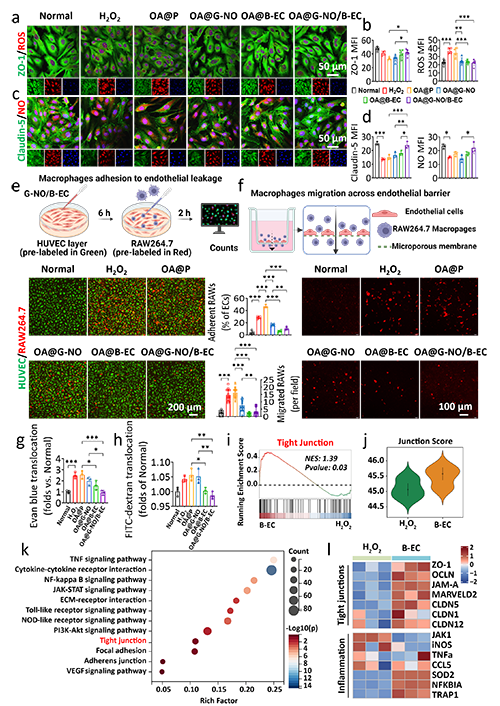
�D3 OA@G-NO/B-EC������Ƥ�g�o���B�Ӻ;��ɼ����B
�������rͿ���D�ơ��S��Ѫ��ͨ����
�ڴ��������}ģ���У�ˮ���zͿ����Ѹ���D�Ƶ����}���ϣ���ԓͿ��δ���MѪС�帽����ۼ����o˨���L�U��30����@ʾ��OA@G-NO/B-ECͿ�ӽMѪ���ٶȷe�֣�VTI������12%��Ѫ�܃ȏ��U��17%��H&EȾɫ�@ʾ������Ĥ��e�p��38%��
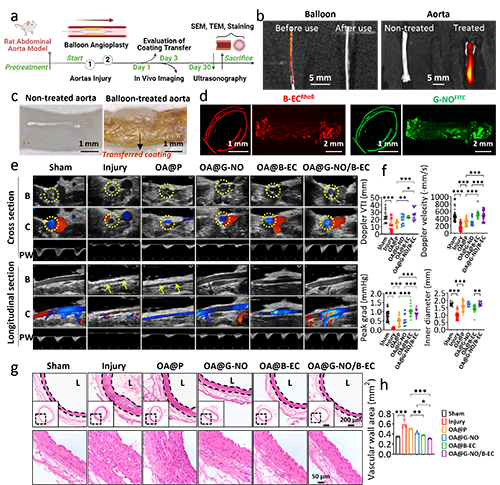
�D4 OA@G-NO/B-ECͿ�������M���w�ȸ������}�U��
�������ك�Ƥ���Ϻ����ޏ�
OA@G-NO/B-ECͿ���@�����M�˃�Ƥ������ֳ�c�w�ƣ�eNOS���ߟɹ�Ⱦɫ�C����Ƥ���w�ʳ�70%�������֏��˃�ƤTJs�ĽY����TJs���ȏ�91.56 nm�֏���17.21 nm���ӽ�����ˮƽ�����������P���ױ��_�ͷֲ�����Ѫ���ޏ��ṩ���LЧ���o��ԓ���zͿ���܉���Ч���M��Ƥ�ޏͣ������װY��������ֹ�٪Mխ��
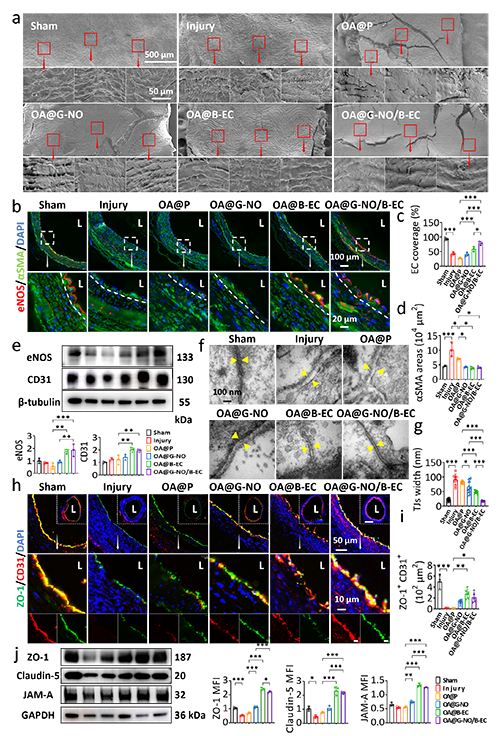
�D5 �����ί��������}�ă�Ƥ���w�����Ϲ���������
���YՓ�cչ����
���о��OӋ������ROS푑�ˮ���zͿ�ӣ�OA@G-NO/B-EC��ͨ�^�p�ӑB���r�I���F�����ί������܅fͬ��ROS�|�lͿ�ӱ��⣬ጷſ������������ROS���ޏ̓�ƤTJs���cNO���w�����M��Ƥ������������TJs���ף�ZO-1��Claudin-5��JAM-M�����_�����̓�Ƥͨ�ԡ������@ʾ��Ϳ������ʹѪ�ܱ���e�֏���������ˮƽ���װY�����@���½�����Ƥ���w��������RNA�y���C����ͨ�^�{��NF-��B/Nrf2ͨ·����Ѫ�ܷ��B��ԓͿ�Ӿ�����Ҫ�D���rֵ���m�䳬��Ϳ��ˇ��Ϳ�Ӻ�ȼ��������ʾ��_�ɿأ��ҿ���չ��֧�ܡ��˹�Ѫ�ܡ����K��Ĥ����е���棬�ƄӾֲ�ˎ���f�ͼ��g�ĸ��¡�
��һ����
�w�o��������ݷ��tԺ��Ƹ�о��T������W��ʿ���㽭��W��ʿ����Ҫ�о��������Ѫ��ֲ������ϼ�������ԣ����և�����Ȼ�ƌW�����㽭ʡ��Ȼ�ƌW�������Ї���ʿ����Ȼ�ƌW����ȶ��������Ŀ��������Ե�һ/��һ������Advanced Functional Material��ACS Nano��Acta Biomaterialia�ȇ��H�����ڿ��l��Փ��10��ƪ���ڙ����Ұl������3헣������W�g����1�¡�������Front. Bioeng. Biotechnol.���徎���Լ�Exploration��VIEW��J. Zhejiang Univ., Sci., A���s־���꾎ί��
ͨӍ����
�����٣������t�W��ʿ�������t������ʿ���������㽭��W������Ƹ�t�����F���㽭��W�������ݷ��tԺ�ăȿ����Σ��㽭ʡ��Ѫ�ܽ����c�����\���о����c��������Σ���Ѫ�܄�����е�㽭ʡ�����о��������Σ��㽭ʡ�t�W���c�W����Ѫ�������t�W���W�Ǝ��^�ˡ��L�ڏ�����Ѫ���R���ͻ��A�о������҇�֪���������K���W���ң��ڏ��s���IJ�����Ĥ�������ί��I������^�ߵ���Ԅ�����I���Ŀ��ЈF�������ȱѪ�����K�������ޏ��ί�����Ѫ�ܽ�����е�Ą����о�������������Ⱥ����և�����Ȼ�ƌW���𡢇������c�аl�Ŀ���n�}��ʡ���c�аl�ȶ���ش�����Ŀ���l��SCIՓ��50��ƪ�����s�@2015����㽭ʡ�Ƽ��M��һ�Ȫ���
�S�G���㽭��W�t�WԺ�������ݷ��tԺ��Ժ�L���㽭ʡ��Ѫ�ܽ����c�����ޏ��о����c�����PI�����A�t�W����Ѫ�ܲ��W�֕�Ů�Խ����W�Mί�T���㽭ʡ�t�W����Ѫ�ܲ��W�֕��ؕ��L���㽭ʡ�t�W��������Ѫ�ܲ��W�֕�ί�T���㽭ʡ�����t�W���̅f�����Ɍ��Iί�T��ǻ��Ӱ���A�W�M���M�L����Ҫ�о����ɼ������}����Ӳ���Mչ�c�����x�Ɂy�����}ǻ��Ӱ��W�c��M�W�о����Ϲ��������և�����Ȼ�ƌW�����㽭ʡ�I���Ŀ���㽭ʡ��Ȼ�ƌW�����㽭ʡ���tˎ�ش��Ŀ���㽭ʡίʡ�������c�Ŀ��헣�ؓ؟�������㽭ʡ���R�������R�����D���о���
���������㽭��W���Ƽ��Tʿ���¼�������������W��ʿ���������Π���W��ʿ�F���㽭��W�t�WԺ�������ݷ��tԺ��Ƹ�о��T����Ҫ���½��ٿɽ�����Ѫ��֧�ܲ���,ˮ���z�dˎϵ�y�ί�Ѫ�ܓp�����Ĥ�������˹�Ѫ�ܼ�ˎ��Ϳ�����ҵ��о����Г��㽭ʡ��Ȼ�ƌW����ί̽�������Ŀ1헣��㽭ʡ�tˎ�l���Ƽ�Ӌ�����ꄓ���Ŀ1헣��㽭ʡ�tˎ�l���Ƽ�Ӌ��һ���Ŀ1헡���5��l��SCIՓ��32ƪ�������Ե�һ����ͬ��һ������Advanced Functional Material�� ACS Nano��Bioactive Materials��Biomaterials��Small��Acta Biomaterialia��Trends in Biotechnoloqy�ȇ��H�����ڿ��ϰl��Փ��8ƪ���Ե�һ�l�����ڙ�l������1헡�
ԭ��朽ӣ�https://pubs.acs.org/doi/10.1021/acsnano.5c05477
- ���ݴ�W�����ƽ��ڈF� IJBM��ؓ�d�~�Ȳ����ݵ��h��푑��zԭˮ���z�ί������ڵ��о��ɹ� 2025-07-14
- �Ϻ��е�һ�����tԺ�RС܊/�|�A��W�΄��� Bioact. Mater.��TME푑��ͺ�ˮ���z��������MYC�����������L�c�D�� 2025-01-17
- �Ĵ���W����|���ڈF� ACS AMI���h��푑��Ͳ���-���S���w�������Ķ��Pickering��Һ���ڸ�Ⱦ���ڵ����� 2024-09-02
- �����������w�Ľܡ������� Small���ۓp����/�迹�c���Ҹ�� fͬ�Ŀɽ����ЙC��ˮ���zͿ�� 2025-05-10
- ����������W���겨���ڈF� ACS Nano: ���ڿ�������W�_�P��ˮ���zͿ�� 2025-03-04
- �㽭��W�w�q���ڈF� Matter���o늇�Ϳ�Ƃ���ˮ���zͿ�����ڸ�Ч���ɳ��m�����l��s 2024-09-24
- �Ї������W�RӾ�ص� Small���ɇ�Ϳ�����ӱ��������z 2025-05-15
