���(d��ng)���ί���PDT���ڰ��Y�ί��I(l��ng)����о�(y��ng)�Ý����������ڃ�(y��u)���Ĺ�W(xu��)���ܺ;ۼ��T��(d��o)��������ROS���a(ch��n)������(qi��ng)���ԣ�����AIE���|(zh��)�Ĺ������[���ğɹ��ҕ�����(d��ng)���ί��б��F(xi��n)ͻ����Ȼ����Ŀǰ����(b��o)����AIE��������Ԯa(ch��n)���ξ��B(t��i)����1O2��������II��������II���a(ch��n)��ROS���^�̌�(du��)�������ه���^�ߣ���ROS�a(ch��n)��Ч�������������[���M���ķ�����r�����֮�£�I�����C�������^�õ��ͷ������ԣ��܉��ڹ��(d��ng)���^���г�������[���h(hu��n)�����������⡣��һ���棬�����ھS�ּ�(x��)�����L���ֿ���(x��)�������������(x��)�������u���D(zhu��n)�������l(f��)�]���P(gu��n)�I���ã���(x��)���˱��J(r��n)���ǹ��(d��ng)���ί�����Ѱ��c(di��n)����ˣ��_�l(f��)����I�ͻ������a(ch��n)��������AIE���������ڴ˘�(g��u)����(x��)���˰���Ĺ��(d��ng)�����Y�ί��wϵ��(du��)�ڿ˷����y(t��ng)������ه��II�������[�����(d��ng)���ί������R�ķ������}����ְl(f��)�]���Ĺ��(d��ng)���ί�Ч������߷�����(sh��)�w�����ί�Ч��������Ҫ���x��
�b�ڴˣ��Ʊ���Ժʿ/���|�����ڈF(tu��n)�(du��)��(b��o)����һ��܉��Ч�a(ch��n)��I�ͻ�������AIE����������䓡�������������푑�(y��ng)�ļ�(x��)���˰����f��ϵ�y(t��ng)�ɹ���(g��u)������������I��AIE���ļ�(x��)���ˣ��������С���������(d��ng)���ί��wϵ��ԓ�wϵ���кõ����������ԡ��ߵğɹ����ȡ���(y��u)����I�ͻ������a(ch��n)�������Լ����õļ�(x��)���˰�����[������Ч�����w����w��(n��i)�u(p��ng)�r(ji��)��(sh��)�(y��n)������ԓ�wϵ�ڹ�����(sh��)�F(xi��n)�˸�Ч�ğɹ����ָ��(d��o)�Ĺ��(d��ng)���ί����܉���Ч��������(x��)������С����w���F(xi��n)���@��������Ч�������D1��

�D1. I��AIE�����[����(x��)���˰�����(d��ng)���ί����O(sh��)Ӌ(j��)���ԡ�
����ͨ�^����ķ����O(sh��)Ӌ(j��)�ͺ��εĺϳɲ��E�������Ƃ�õ��ɂ�(g��)��ӽo�w��D��-���w��A����(g��u)�͵�AIE����TFMN��TTFMN�����߾����F(xi��n)����t/���t��ɹ�l(f��)�䣬�ҷ��ӽY(ji��)��(g��u)����Ť����TTFMN���F(xi��n)�����郞(y��u)����AIE���|(zh��)�����⣬����TTFMN���и�С�Ćξ��B(t��i)�����B(t��i)�ܼ�(j��)���ES-T������ROS�a(ch��n)�������h(yu��n)��(y��u)��TFMN���о�������TFMN��TTFMN��Ҫ�a(ch��n)��I�ͻ������u�����ɻ���?OH���������a(ch��n)��II�ͻ�����1O2����TTFMN���F(xi��n)�����ѵ�?OH�����������D2��������(j��)Weller��ʽ�ͼ���˹������׃��Ӌ(j��)��Y(ji��)���������M(j��n)һ���C��(sh��)�������B(t��i)��TFMN��TTFMN�������ȏĭh(hu��n)���еĚ������õ���ӣ��ٌ�����D(zhu��n)�ƽo�����B(t��i)������õ�������x�ӣ�?O2?�����S��(j��ng)�^һϵ�ж���(j��)����(y��ng)��K�a(ch��n)��I�ͻ�����?OH��
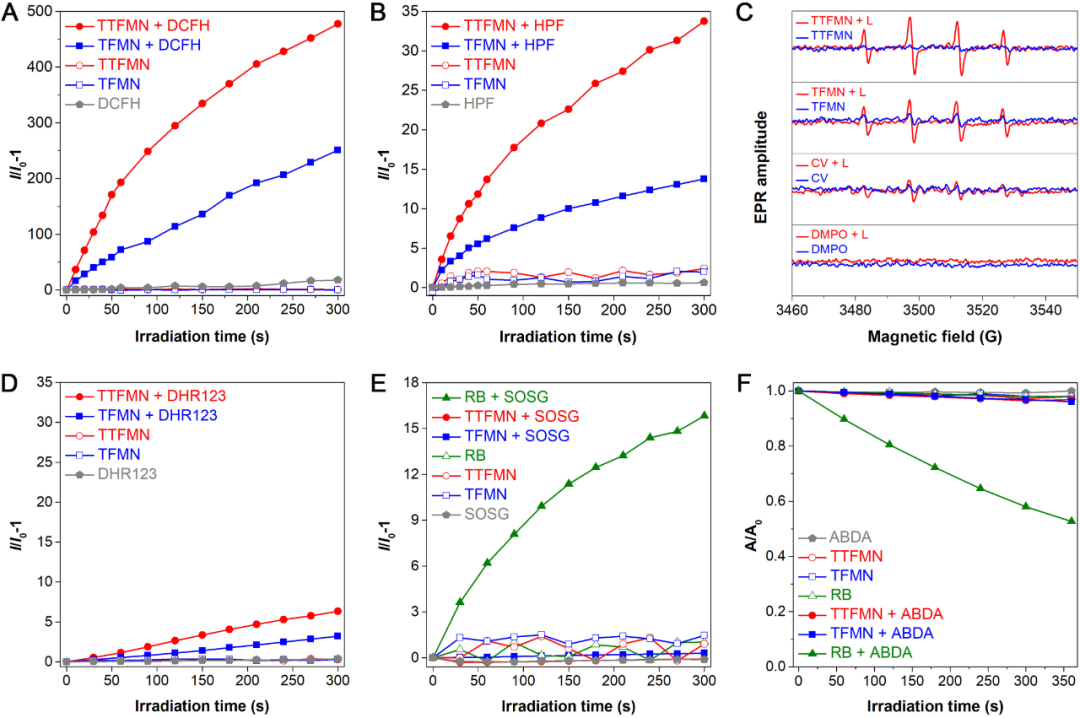
�D2. AIE���������a(ch��n)��������������
�錍(sh��)�F(xi��n)I����TTFMN�ļ�(x��)���˰����f�ͣ����߽�����푑�(y��ng)�ļ�(x��)���˰����ģ�TAT����ă��H���d�w��TTFMN�����Ƃ�õ�TTFMN-NPs���w����w��(n��i)�u(p��ng)�r(ji��)��(sh��)�(y��n)��������TAT������(d��o)�£� TTFMN�܉ɹ��f������(x��)���˅^(q��)�D3���������ڹ�����ͨ�^���[����(x��)����ԭλ�a(ch��n)��I��ROS�T��(d��o)�[����(x��)�������������[����(x��)����ֳ��Ѫ����������K�l(f��)�]�@���Ŀ��[�����ã��D4����
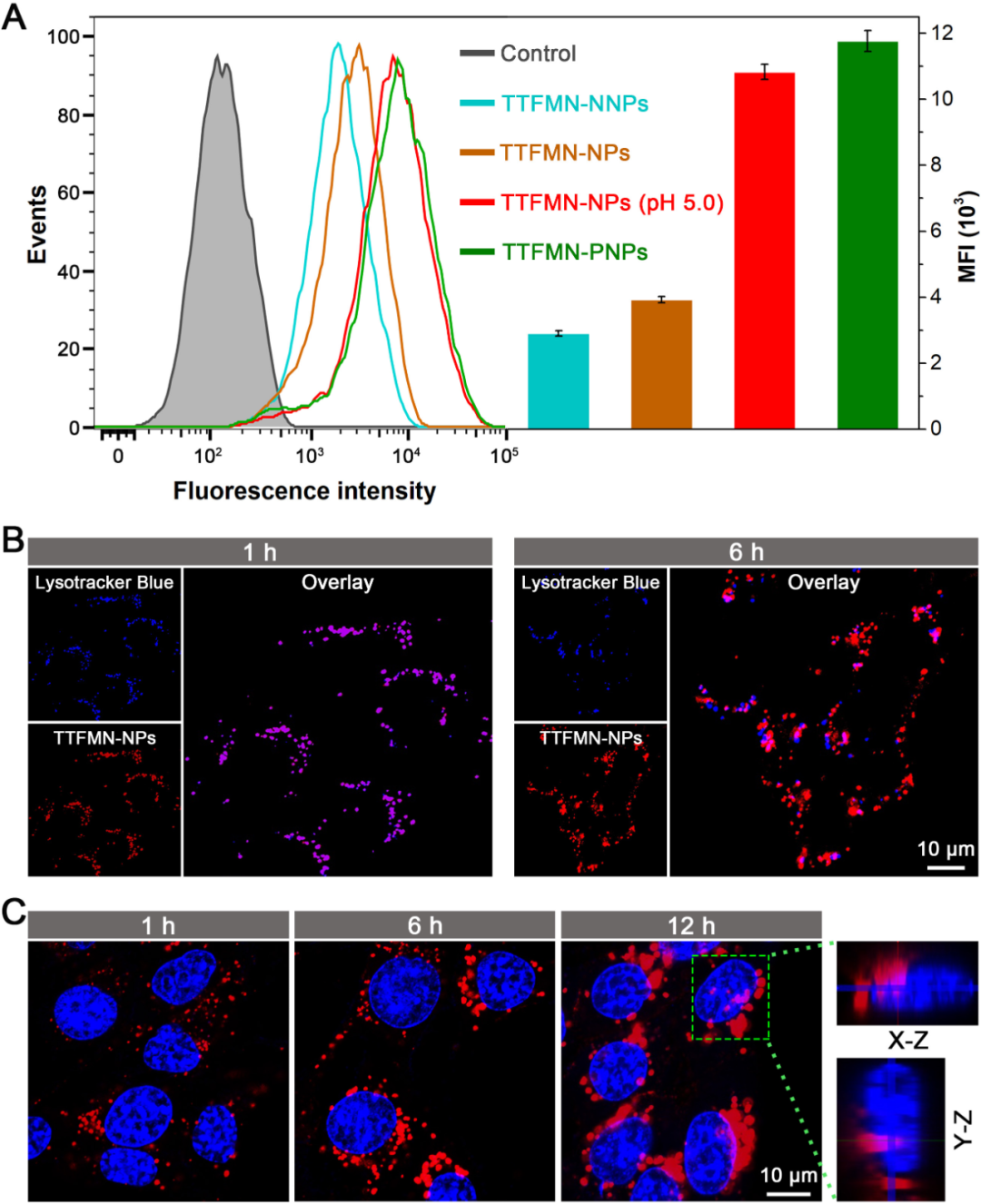
�D3. ��(x��)���zȡ����ø�w���ݼ���(x��)���˰��������о���

�D4. ���w�ɹ����ָ��(d��o)�Ĺ��(d��ng)���[�����������о���
�@�(xi��ng)�о��ǻ���AIE���ӵļ�(x��)���˰����I���(d��ng)���ί��ijɹ��������@�N����ġ�������ڵ����ϡ��IJ����������[�����(d��ng)���ί�Ч���ĘO��������������һ��I��AIE�����O(sh��)Ӌ(j��)�_�l(f��)�Լ���ϵ�y(t��ng)�f�͵ļ�(x��)���������\���wϵ�Ę�(g��u)���ṩ���O(sh��)Ӌ(j��)˼·�͌�(sh��)�`��(j��ng)�(y��n)�����P(gu��n)�о�������ǰ�ԡ�Good Steel Used in the Blade: Well-Tailored Type-I Photosensitizers with Aggregation-Induced Emission Characteristics for Precise Nuclear Targeting Photodynamic Therapy�����}�l(f��)����Advanced Science�ϣ����µ�һ���ߞ����ڴ�W(xu��)AIE�о����������粩ʿ��ͨӍ���ߞ����ڴ�W(xu��)AIE�о��������|����������ۿƼ���W(xu��)�Ʊ���Ժʿ��
���(xi��ng)Ŀ�@���ˇ�����Ȼ�ƌW(xu��)����51903163, 21801169�����V�|ʡ�ܳ�����ƌW(xu��)����2020B1515020011�����Ї���ʿ��ƌW(xu��)����2019M653036���������пƼ�Ӌ(j��)����JCYJ20190808153415062, JCYJ20190808142403590�����(xi��ng)Ŀ���Y����
Փ��朽ӣ�https://onlinelibrary.wiley.com/doi/10.1002/advs.202100524
- ������Ĵ�W(xu��)�����ڣ��Ʊ���Ժʿ/�w�����ڈF(tu��n)�(du��)��ACS Nano������(x��)��Ĥ����ľۼ��T��(d��o)�l(f��)�����������(j��ng)ۙ�͓p���Ŀ�ҕ�� 2025-01-21
- ������Ĵ�W(xu��)�����ڣ��Ʊ���Ժʿ�c�w�����ڈF(tu��n)�(du��)��ACS Nano���C�����ۼ��T��(d��o)�l(f��)����ό�(sh��)�F(xi��n)�߷ֱ�������� 2025-01-07
- �������Ʊ���Ժʿ/�������賯 AM������AIE���Լ{��(f��)��ˮ���z�Ŀɴ�������ʽ��Ϣ-���в��� 2024-03-23
- �Ʊ���Ժʿ/���|������Biomaterials��ؓ(f��)�dAIE���ļ{���w�S��Ĥ���ڹ��(d��ng)�����Ч��(y��ng)�f(xi��)ͬ��������o(h��) 2021-07-19
- �A��������W(xu��)�Ʊ���Ժʿ�F(tu��n)�(du��)��־���о��T�n�}�MAFM���ھۼ��T��(d��o)���ɻ����ķ����O(sh��)Ӌ(j��)���䷦���[���ί���(y��ng)��ȡ���M(j��n)չ 2020-08-18
- ��������˹-�Rِ��W(xu��)������ڈF(tu��n)�(du��) AM: ����ģ�K���ԽM�b�����Ӽ{��̽�ͨ�^�˴Ź����˴Ź���/���t��ɹ����z�y���ٰ� 2023-12-13
- �Ʊ���Ժʿ�F(tu��n)�(du��)/�Ͽƴ���P�����n�}�M ACS Nano����������\��Ч���ġ�һ�wʽ�����t��l(f��)��{�ۼ��w 2023-03-04
�\���P(gu��n)ע�߷��ӿƼ�

- ����(b��o)���C(j��)��(hu��)��500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ�(hu��)�h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��(hu��)
- �Ј���300�|��PMEC China ɫ...
- ����ע��(c��)��2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �������S���e���ڈF(tu��n)�(du��) Angew...
- ���ϴ�W(xu��)����/�S�M(j��n)�F(tu��n)�(du��) AFM:...
- ���T��W(xu��)�������n�}�M Sci. ...
- �A���r(n��ng)�������/����...
- ��h�������l(w��i)�ֽ��ڡ���P��...
- ��ʿ�m��W(xu��)�������F(tu��n)�(du��) Adv. ...
- ��h��W(xu��)�������ڈF(tu��n)�(du��)��Adv....
- ��������Rͬ�c���ڈF(tu��n)�(du��)��Sc...
- �Ϲ����غ������đ�Ƽ/�п�...
- ���T��W(xu��)�ܱ���F(tu��n)�(du��) ACS Nan...
- �V����W(xu��)���P���ڈF(tu��n)�(du��) CEJ...