UCLAꐿ����� Chem. Soc. Rev. ����: ���ڂ��Ի��t�������ĉ�늼{�װl늙C


���ԉ�늼{�װl늙C�İlչ���^ȥʮ���н��v�˿��ٰlչ�������ڳɞ�δ�������M�Ă��Ի��t�������ļ��g���A���������Ч�ęCе������D�Q�����ڌ�ʩ���Թ�����ԣ��@Щ�O�������ӂ��С�늴̼��ί��Լ����w�������W�����ռ��I���M�д������µ��t���������á�����ȫ���������ڂ��Ի��t�������ĉ�늼{�װl늙C��PENG�����ں�Ҫ��B�ˉ��Ч���Ļ��Aԭ��֮��߀ϵ�y��ӑՓ�˲��Ϲ��̲��ԡ������Y���OӋ�Լ������w�����ĵ������ռ������к��ί����á����⣬߀Ԕ�����������É�늼{�װl늙C�M���Թ��������ӌW�͂��Ի��t������������͙C����
�S�����к���Ϣ�W�j���g���@���M�������W���پ�������Ӌ��C���֙C�Ȃ��y�����O���ό��F����ͨ������µļ��gƽ�_Ҳ���Ԍ��@Щ���������Uչ���ճ����w�͂��ˣ�����u�γɺ��w�������Խ��Խ�ͬ��������W (IoT) ��ʽ�����d�ļ{���g�Ͳ��ϿƌW����Ҳ�Ƅ�������������ӌW�İlչ���Y�����Wƽ�_�����ܿɴ����O���яV�������ڽ����O�y���˙C�ںϡ��˹����ܺ��S���������á�ԓ�I���ѳɞ�ƌW����I�����A�������w���f���S�� 5G ���g�Ŀ��ٰlչ���ɴ���������ӿ�����B���γɂ������W�j���Ķ��邀�Ի��t���ṩ�����죬�������h���������Ӱ푡���������S���t���������\��ģ����u�����tԺ�������D���Ի��ߞ����ģ��O��ش��M�˿ɴ���������Ӽ��g�ڂ��Ի��t����������İlչ�����Ƶ����Կɴ��������������ڱO�y���w��ӣ������w����������ڠ���@�ӵĂ�Ⱦ�����邀���ṩ�˟o�������������ĄӑB�����u���͂��Ի��t����
�ɴ���������ӌW�܉�ǰ�Լ����ί������ĵ��t������ϵ�y�D׃���Լ����A���ͽ����O�y�����c�Ă��Ի�ģʽ�����У��ɴ������������ԏ����w���@�Ѓrֵ����Ϣ���F���w�����O�y���dz�����t�����W (IoMT) ϵ�y�ĺ��ĽM��֮һ��Ȼ�������@Щ�ɴ����O���ṩ���m�������Դ��Ȼ��һ���ش����𡣂��y�ϣ��˜ʹ�늷�ʽ��ه��늳أ�����O����䪚���Դ�Ԍ��F�����\�С���Ч������������һ�N�������_�l�Թ�늂��������������������е��������W�������磺���w��ӡ����K/���\�ӡ�ѪҺѭ�h����ʽ�����@Щ�����D������ܣ��A�ڌ��ɴ����O���c���y늳ص����މ������l�����Q����x����K���S�����Թ�늲������e�nj���ֲ��ʽ�O�䣬�Թ���O�������Ч��ֹ��Ҫ���Q�Դ�Ķ������g���ṩ�˾�ă��ݺ���Ҫ�đ���ǰ����
�ЎN���g���Ԍ��@Щ�������W���D������ܣ������������ډ��Ч����PENGs����Ħ���Ч����TENG��,�ŏ���Ч����MEG������늴�Ч�������У����ډ��Ч���ĉ�늼{�װl늙C��PENGs���� 2006��l���ԁ���������е����Զ������Pע�����鉺늲��ϣ�PENGs���к��εĹ��̽Y�������Ԍ��F�Cе�ܺ���ܵĿ����D�Q�����F��Ч�ęC���ϡ�����푑���PENG ���H�������������ռ�����߀�����ṩ���ӂ��������������|�X���С�������׃���С��W���е���ʽ�������������w�ϕr��PENGs ���ԱO�y���w��ӵ���������̖�������}���z�y�������O�y���M������ģ��Ӌ�㡢Ѫ���O�y�ȡ������@Щ����֮�⣬�a�������߀�V������ԭλ늴̼������������{�����M��������ˎ��ݔ�͡���������S���²��ϵij��F�S���¼ӹ����g�İlչ��PENG���g�lչѸ�٣�����Դ�����к��ί��I��ȡ�����ش��Mչ��
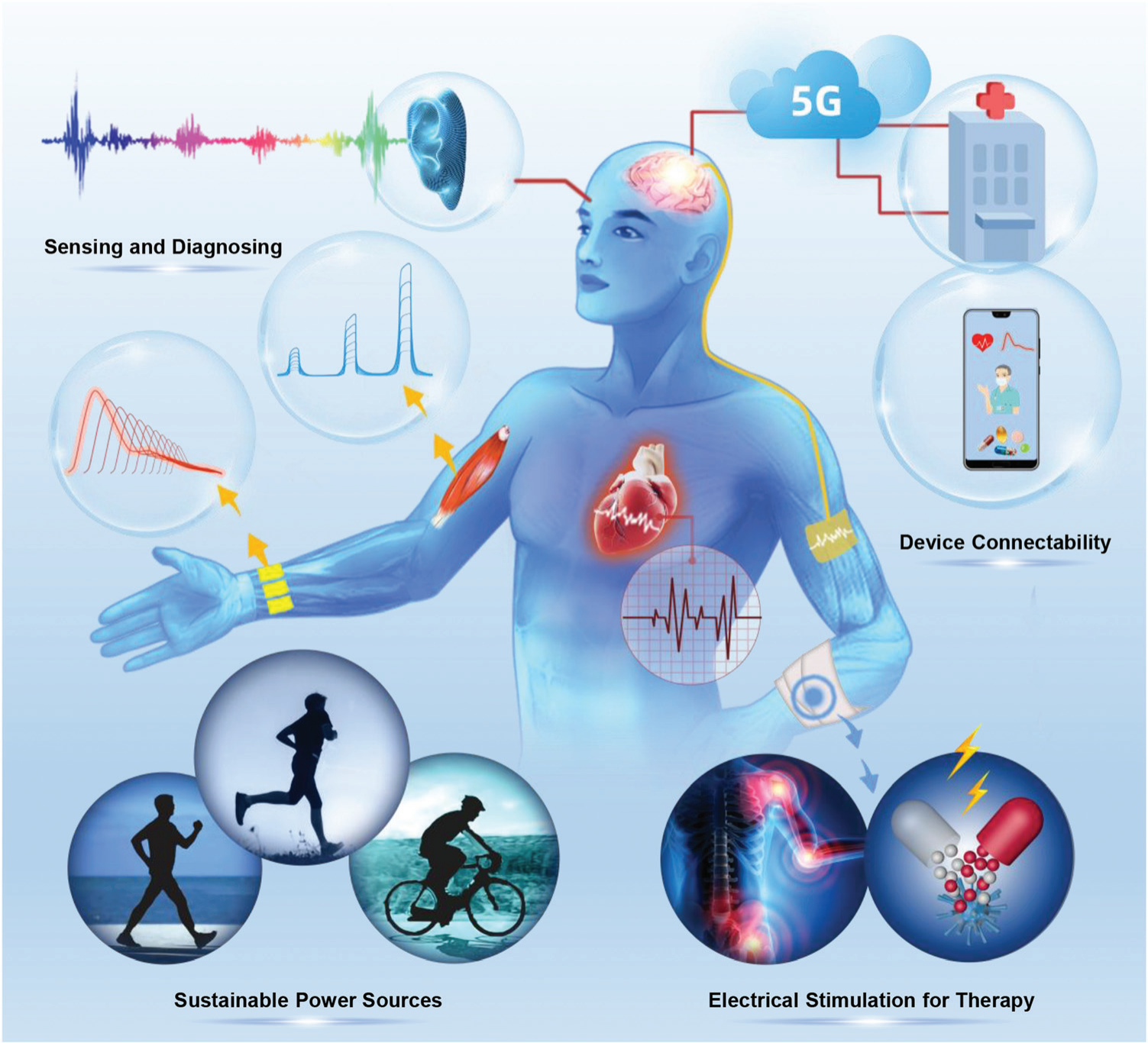
���C��ּ��ͻ���ͺ��w����Դ�����к��ί������I��Ľ��� PENG �Mչ�����c�Pע���ڂ��Ի��t�������е������t�W���ã��D 1�������˸��õش��M�� PENG �������t�������еđ��õ����⣬�����_ʼ�����Ҫ��B��PENG�Ļ��A��������ԭ�����S��B��һЩ���͵ĉ�늲��ϣ������o�C���ϡ��ЙC���ϡ���늏ͺϲ��Ϻ���Ȼ��늲��ϡ��Mһ�����w�˸��N���ډ�늲��ϵ�������ӌW���о��Mչ�Լ��F�������е������t�W���ã��������w�����ռ������к�늴̼��ί��������һ���У�Ԕ�������ˌ� PENGs ���ڂ��Ի��t������������͙C����

�D 1�����ڂ��Ի��t�������� PENG���������w���P�������ռ����Թ�늂��к�늴̼��ί���
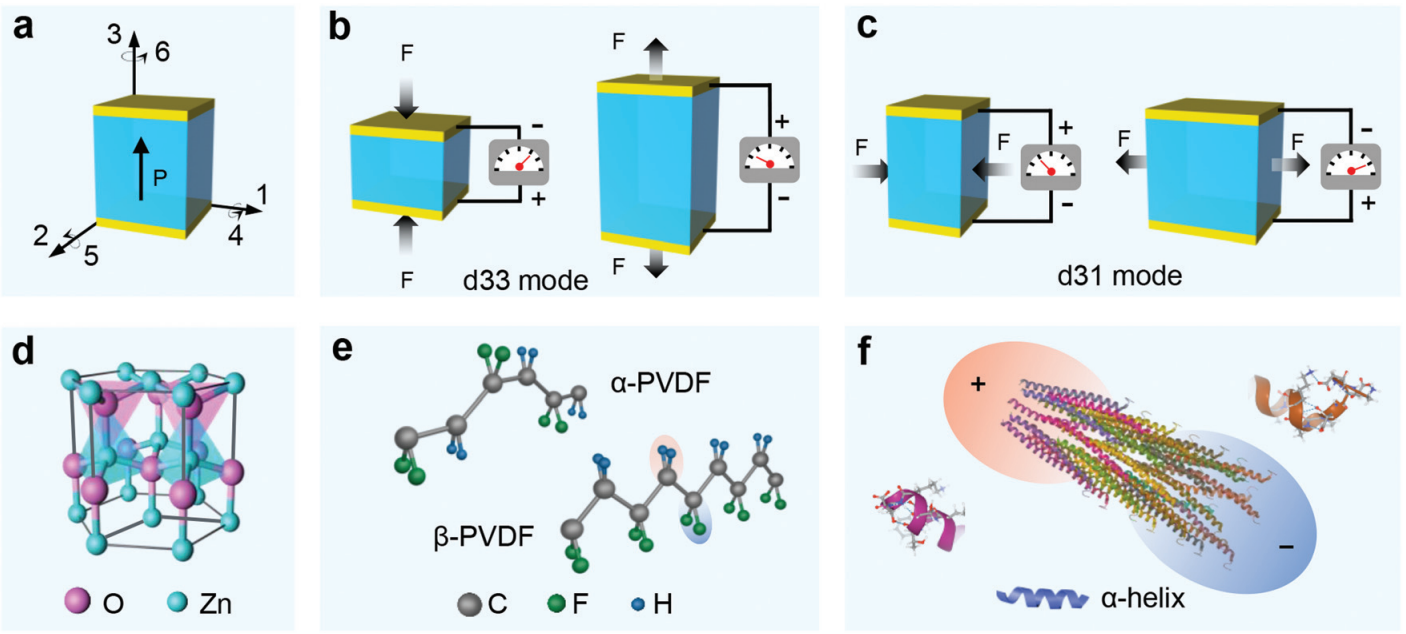
�D 2����늲��Ϻ͉���ԡ� (a) Ӱ푉��Ԫ�������ķ���d33 (b) �� d31 (c) ����ģʽʾ��D��(d)�o�C��늲���ZnO���w�\�V�Y��ģ�͡�(e) �ЙC��늾ۺ��� PVDF �� �� ��� �� ��Y����(f) M13 �ɾ��w����Ȼ��늲��ϡ�
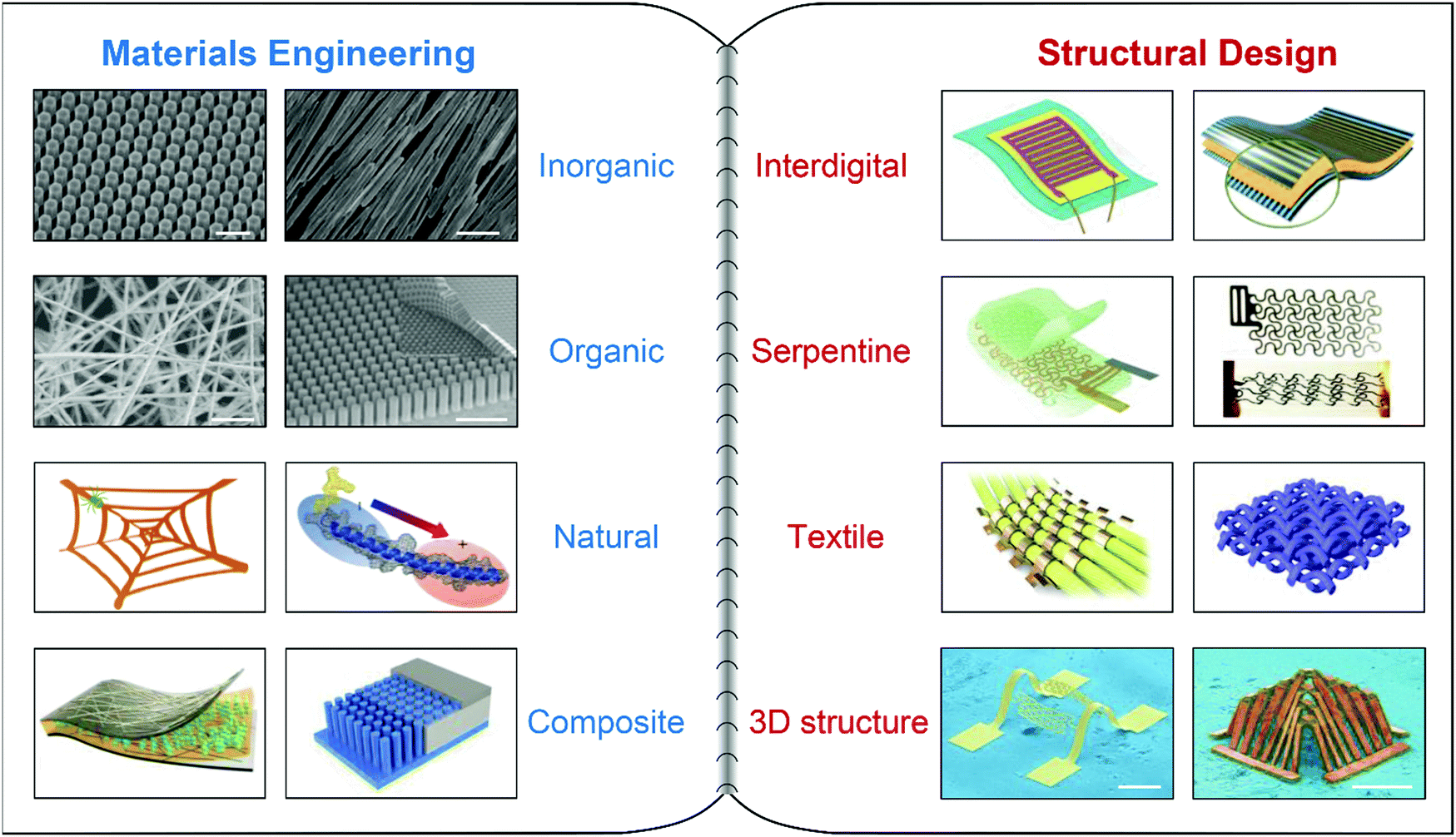
�D3 PENGs�IJ��Ϲ��̺ͽY���OӋ���o�C���D���� ZnO �{�װ��� SEM �D���������ߣ�2 ��m���M�b������{���� SEM �D���ң��������ߣ�10 ��m���ЙC�PVDF �{���w�S�� SEM �D���������ߣ�5 ��m��P(VDF-TrFE) ���� SEM �D���ң��������ߣ�30 ��m����Ȼ��֩��z�Y��ʾ��D�������⚤����ʾ��D���ң����ͺϲ��ϣ�չʾ PVDF-����}�� PENG �Y����ʾ��D����ʾ��D��ʾ���� P(VDF-TrFE)/BNNTs �{�ͺ����� PENG �ĽY�����ң������w��PENG ʾ��D�������н���늘O�� PENG ʾ��D���ң��������������� PVDF ��Ӽy����ʾ��D������Ƭ���ң�������Ʒ������ PVDF �ļ���Ʒʾ��D�������� PENG ��ʾ��D���ң���3D �Y�������̈́��� PVDF ���^�Y�����͎�늘O�� 3D PVDF ���^�Y�����ң��� SEM �D�����ߣ�500 ��m��

�D 4 ���ڟo�C��늲��ϵ������ռ��� (a) ���� ZnO �{���� PENG �B�ӵ����ʳָ������ָ������ʾ��D��(b) PENG �� I-V ���ԡ���D�f���� PENG ��ʾ��D�����P�ڜy��ϵ�y���B�����á�(c) ����ָ�����Ե��؏����r��PENG �a�����_·늉���(d) ʹ������ PZT �����ռ����Ŀɴ������õ�ʾ��D��(e) ʹ�� LLO �����Ƃ����� PZT ��Ĥ�� PENG �Ĺ�ˇʾ��D��(f) ����ӏ��������� PZT �����ռ�������Ƭ�������ߣ�1 ���ס�(g) ����ָ�����ĉ�늏ͺϲ��ϵ���Ƭ�͏��ԹǼ��ω�늏ͺϲ��ϵęM���� SEM �D�����ߣ�50 ��m��(h) ��ֲͬ�벿λ��ʾ��D��(i) ���Բ�ͬע��λ�c�Ĵ����ϣ��Ͳ����£�ģʽע��� PENG ��ݔ�����ܡ�
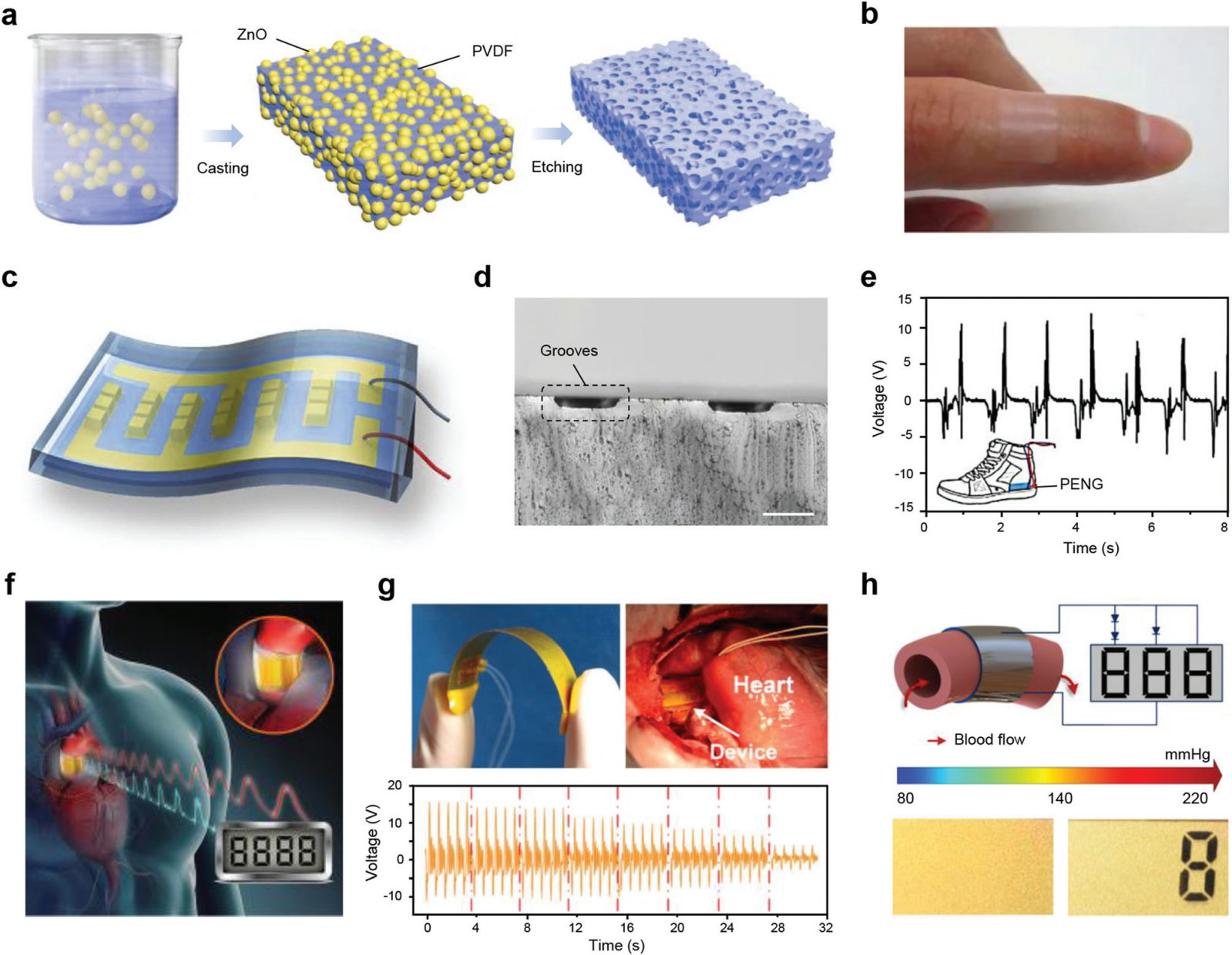
�D 5 �����ЙC��늲��ϵ������ռ��� (a) �Ƃ���� PVDF ��Ĥ��ʾ��D��(b) ճ������ָ����Ľ�� PVDF ��Ĥ����Ƭ��(c) �������еļ{���w�S�� 3D ��ָ늘O�� PENG ʾ��D��(d) PDMS �а��ۙM������@��Ƭ�������ߣ�500 ��m��(e) �������ߵ��ˮa����ݔ��늉���(f) �����������}�ϕr���w��ʹ�õ� PENG ʾ��D��(g) ԓ�b�õ���Ƭ�@ʾ�����g�Բ��������i���������}�ϣ��ϲ�����������ݔ��늉��S��ͬ�ĉ������ö�׃�����°벿�֣��� (h) �տs������ 140 mmHg �r PENG �c�� LCD ��ϵ�y�D����Ƭ��

�D 6 ���ډ�늏ͺϲ��ϵ������ռ��� (a) 3D ���B����մ���ĭ�� PENG ��ʾ��D��(b) ����e 3D ��늏ͺϲ��ϵ���Ƭ�������ߣ�5 ���ס�(c) 3D��늏ͺϲ����ڲ�ͬ���쑪׃�µ�ݔ��늉���(d) ������� �� ���γəC�Ƶ�ʾ��D��(e) �˚���늼{���w�S�� TEM �D�����ߣ�500 nm��(f) �����Ƥ�w��Ԫ��ʾ��D��(g) ���ڷ� PZT �մɿ�ܺ� P(VDF-TrFE) Ϳ��Ĥ�� HIPT �ͺϲ��ϵ�ʾ��D�����~�W����늘O��(h) ���� 3D ���늘O�Ļ��� Sm-PMN-PT �� PENG ��ʾ��D��(i) �����P���\�������ռ����������Ƥ�w�ĸ�����C�f����

�D 7 ������Ȼ��늲��ϵ������ռ��� (a) ���ķN�Ȱ����M�����﹤�����ĉ�� M13 �ɾ��w�Y��ʾ��D���� b ��ͨ�^�Όӵ��S�������L�����S�C���ż�O�ӵ��ɾ��w�ĉ�����Ե�ʾ��D��(c) ��ֱ���е� M13 �ɾ��w�M�b�ď��ƝBʾ��D��(d) �ɶ��ģ���е��؏͝B���Ƶ��ɾ��w�{�����γɵ�ʾ��D����e��֩��z�Y��ʾ��D������Ȼ֩��z�� SEM �D�����ϣ��������ߣ�20 ��m��֩��z�ĵ��ΈD�����£���(f) PENG �����������®a����ݔ��늉���(g) 3 ������Ԫ�a������������c���Gɫ���{ɫ LED��(h) �ǘO�� ESM �ĘO����늈�������(i) �c�������P��ݔ��늉���(j) ��Ƭ��С�ĉ�늸ʰ���-PVA ��Ĥ�Ĕ��a��Ƭ��
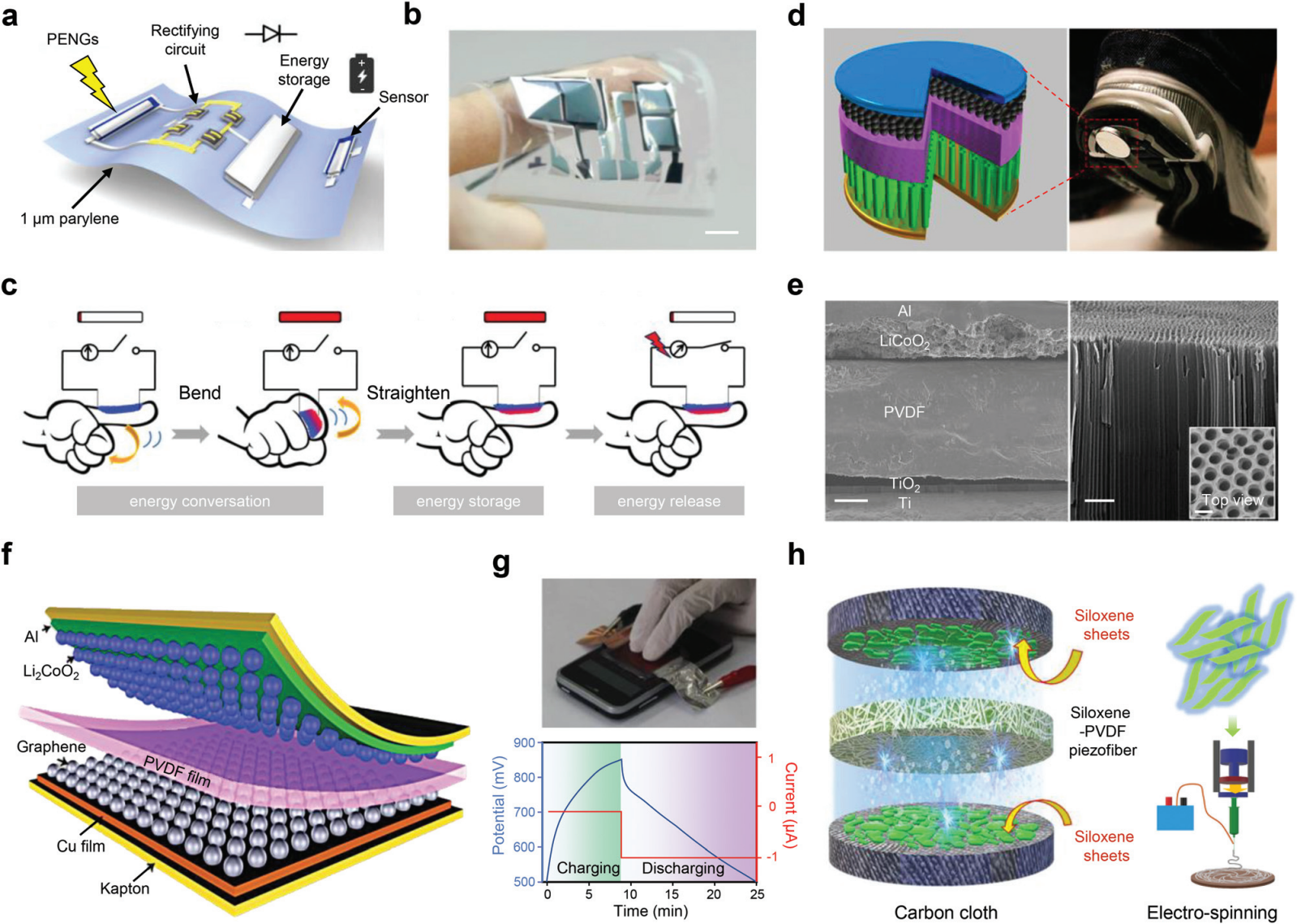
�D 8 �����ռ��ʹ惦�ļ��ɡ� (a) ������ 1 ��m ���ی����ױ������ϵ�һϵ�г����������ķ�����(b) �����ռ��������W�����ij����� PENG ����Ƭ�������ߣ�1 ���ס�(c) �{�ͺ�Ĥ�������\���µ������D�Q�̓���ʾ��D��(d) PENG����x��늳ػ�ϵ��Գ��늳ؽY���OӋ��(e) �Գ��늳صęM���� SEM �D�����½ǣ��������ߣ�30 ��m�����R�� TiO2 �{�ܵķŴ�D�����½ǣ��������ߣ�1 ��m����D�Ǽ{�ܵ��ҕ�D SEM �D�����ߣ�200 nm��(f) �@ʾ�����Գ��늳��OӋ��ʾ��D��(g) ͨ�^��ָ������늵������Գ��늳ص���Ƭ���ϲ�����һ�����͵��Գ�늺������ķ���^�̣��D����(h) ���ڹ�������Գ��늳ص�ʾ��D��

�D 9 �������w�\�ӸБ��� PENG��(a) �����{�װl늙C����ۙ�����\�ӵ��Թ��Ƥ�w��������(b) �څ��c���M���沿������������Ę�a�鴤���r����Ƥ�w��׃����ȵĈD���@ʾ��׃�D��������c��ʹ�Â��������Ͳ�ʹ�Â��������ң��ĽY��ʾ�����@ʾ��С����׃��픲������������׃���ײ�����(c) ���ډ���մɼ������i���\�Ӯa�������̖�Č��Y����(d) �༉���X��ꇵ�ʾ��D��(e) ���������ϵ����ж�����������Ƭ�D�����ڲ��֏�������ָ̧����\�ӣ��ψD���������Ă�����̖���D����(f) �������ڸ��N�����\���µ�ݔ����̖��(g) ���ڼ����О�O�y�����S�ּ��i PVDF/ZnO �w�S�� PENG ʾ��D�������ߣ�1 ��m��(h) ��ͬ���з����С�ȷ������ȣ����ȣ��c��һ�lС�ȷ������ȣ����ȣ��ı�ֵ��
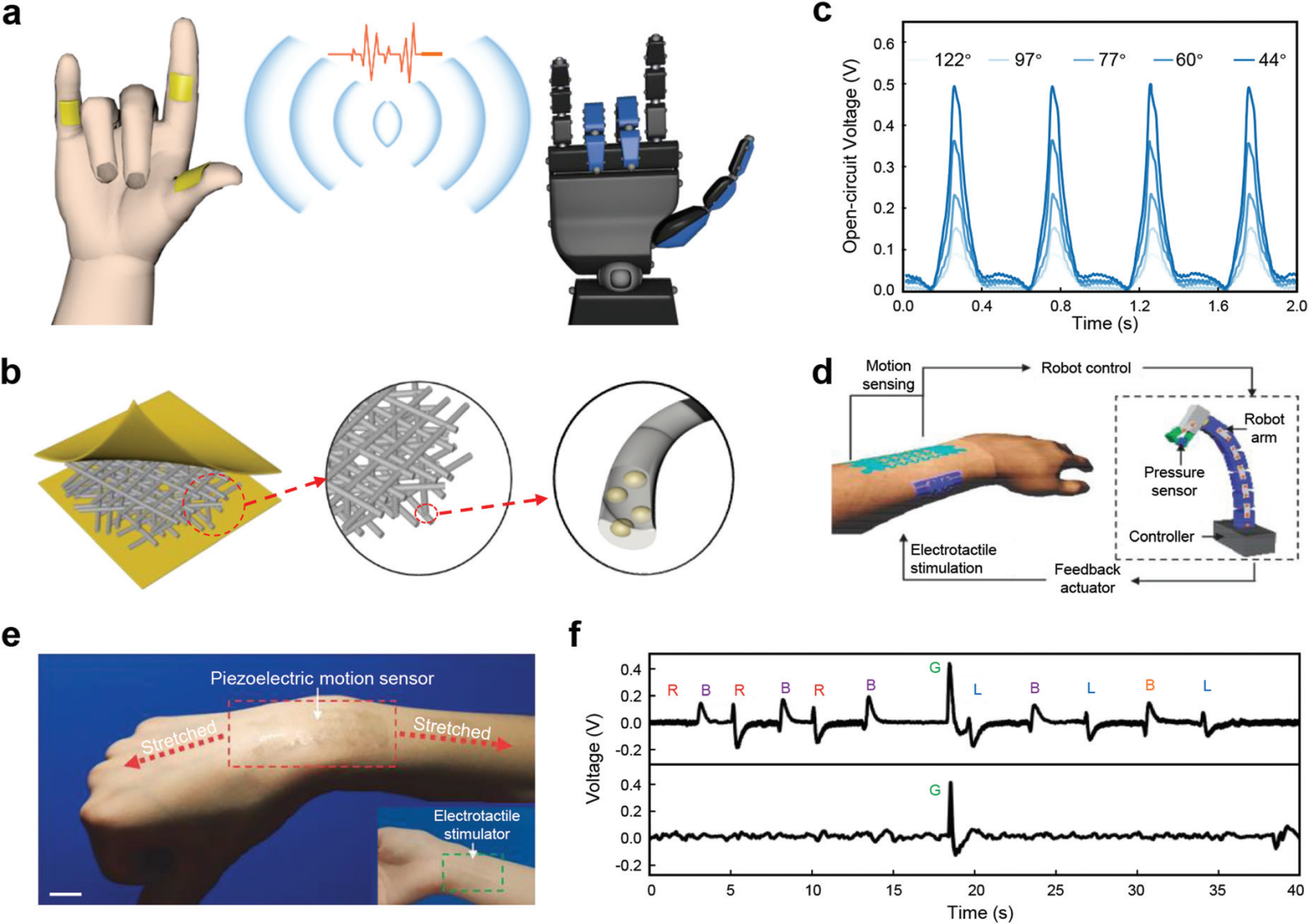
�D 10 �����˙C������ PENG�� (a) ���������Y���� PVDF/ZnO �{���w�S���Թ�늉�늂�����ʾ��D�������h�̿����քݡ�(b) �����{���w�S��Ĥ�͆θ��{���w�S���OӋ�b��ʾ��D��(c) �Բ�ͬ�Ƕȏ����a�����_·늉���(d) ����ʽ�˙C�����]�hϵ�yʾ��D��(e) ������\�ӂ���������|�X�̼����ĈD��D���������ߣ�20 ���ס�(f) �����\�ӂ���������һ�У��͊A���ϵĉ������������ڶ��У��@ȡ�ęz�y��̖��
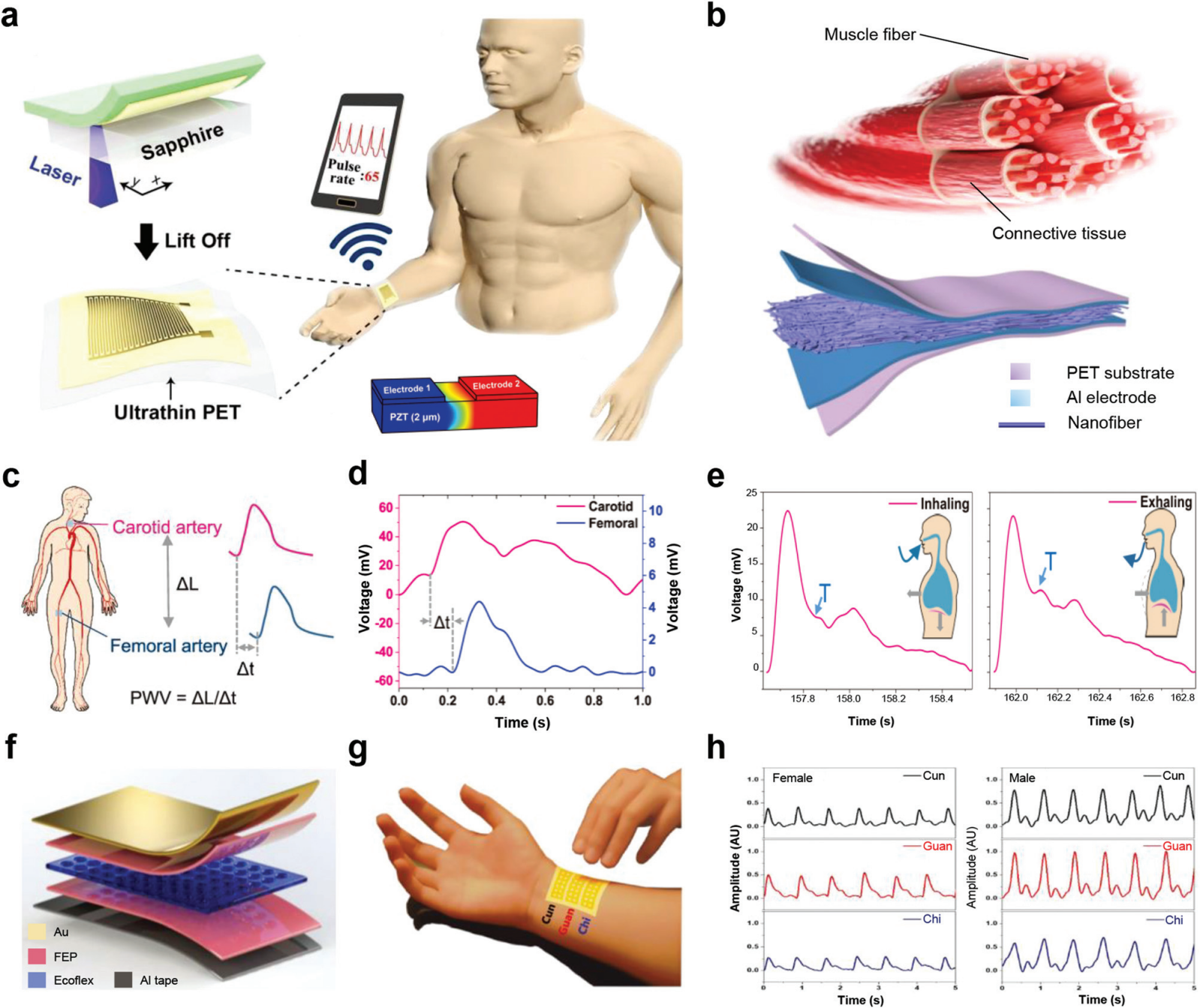
�D 11 ���������w�����е� PENG�� (a) ���� PZT ��Ĥ���Թ�늉����������������^��ʾ��D���� b ���ɽY���M�������ļ����w�S���Ƴɵļ����w�S���l��늼���Ʒ��ʾ��D��(c) PWV Ӌ��ʾ��D��(d) ���� PWV Ӌ����i�Ʉ��}�}�����Ρ�(e) ������^��������ͺ������g���ń��}�}�����Ρ�(f) ʹ�� FEP/Ecoflex/FEP �A�ӽY������v�O�w��Ĥ���}�_�����b��ʾ��D��(g) ģ�M�挍�t���Ă��y���t�}���ɼ�������ʹ����ָ�c�}���Б�ϵ�y�ڴ硢�P����λ�á�(h) �քe��Ů�Ժ�����־Ը���ڴ硢�P�ͳ�λ�Üy���ĵ����}�����Ρ�

�D 12 �����w���������W���е� PENG��(a) ���ھ������������ܘ��� 3D ��ӡ���ԉ�늾���ğo���ԸБ�ȭ������ʾ��D��(b) ���Ĺ�W�D���������С�Ŀ��g�ֲ��������քeͨ�^ֱ�Ӵ�����ҹ�ȭ���Љ��ڕr��(c) ���ډ�ӡ P(VDF-TrFE) ����е����ԉ�����S�|�X������ʾ��D��(d) ���S�|�X�������ڷ������ͼ������µ�ģ�M��(e) �����Թ���㲿������������е���Ƭ�́������w�ĉ����ݵĶ��S�ȸ߾��Dӳ�䡣(f) ���г��̈́��ȵ� 3D �г߶ȉ�늿�ܡ���g���ڴ���e��픲�����С��e���ײ���ʩ�Ӊ������b��ʾ��D��(h) ��ƽ���^����ʩ�Ӳ�ͬ���������ɫ�������ĕr��ݔ��늉�����ɫ��������

�D 13 �����w���������W���е� PENG�� (a) ���� PZT �{����ģ���������ķֽ�ʾ��D��(b) ϵ�yʾ��D��ǰ����Ƭ�������͎����b�O�䣩��(c) ���Ԍ��Ĵ����Ԕ����������ߣ�2 ���ס�(d) ���ڳ��� PZT �������͂��������O��ʾ��D��(e) �����b�ã������ߣ�5 mm���ͷ���������M���ϵ��b�ã��ң������ߣ�2 mm���Ĺ�W�D��(f) ���w�����w��ģ���y���Ĺ�W�D��ͽY���Լ���ጺ���ͬ���ٵ��x�w�Y���������ߣ�1 ���ס� (g) ��ֲ��������ڽM�����i���K������ĝ��ڑ��á������ߣ�1 ���ס�(h) ��ͬ�������i���K�ς�������늉�ݔ�����Լ����ƽ�_�ϵ��}�_�����������ݔ�루�ײ������s�����iģ�ͣ��ϣ����w���u���Дz��ţ��ǰ���늉�ݔ���D��(i) ���� PZT �Ă������cθ�Ƚ�Ƥ�ȸQ�Rθ��ڹܵ���Ƭ�������ߣ�1 ���ס�

�D 14 ���ں�Һ���е� PENG�� (a) �Ă����ں�Һ�������Թ�늿ɴ����o�����������І�Ԫ��(b) �Թ�늿ɴ����o�����Ƥ�w�ęM���O��ܘ��D��(c) �Թ�늿ɴ����o�����Ƥ�w�Ĵ�ֱ�O��ܘ��D��(d) ZnO �{����к͘�Ӄɂ� Ti 늘O�Ć� ZnO �{���� SEM �D�����ߣ�10 ��m��(e) ���� ZnO �{���ڼ�ˮ��ͨ�^ʩ��׃�ήa���ĉ���λ��(f) �����w���w��yԇ�ķ����M�б��^��
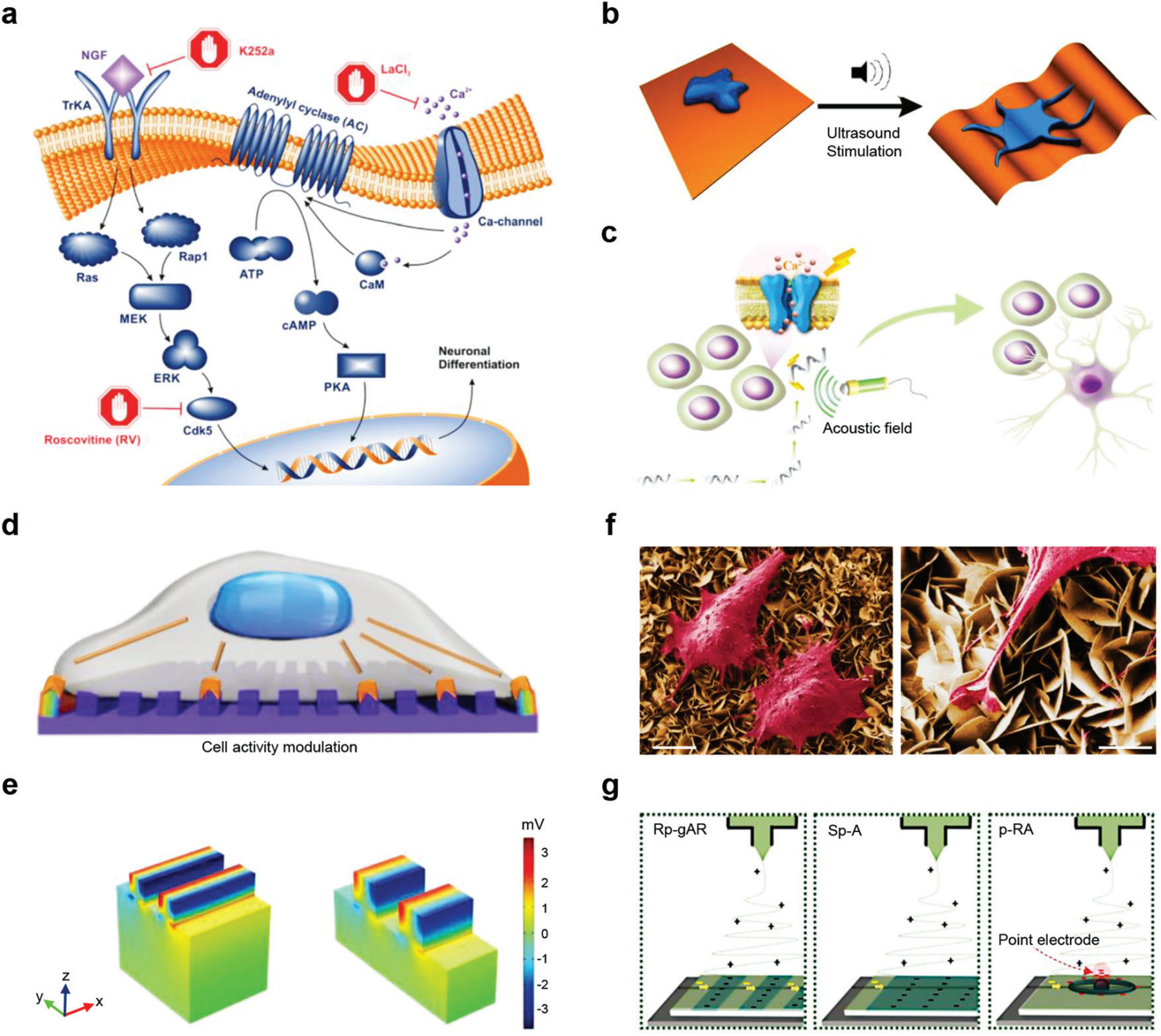
�D 15 ���ڼ��������{���� PENG�� (a) �f��Ӱ� PC12 �ֻ��ļ�����;����(b) ��� ��-PVDF Ĥ�ij��̼�ʾ��D���T�� PC12 ��������Ԫ�ֻ���(c) �߶ȿɿ�늙C�T��Ŀ���ɼ����ֻ���ʾ��D��(d) �ھ��м{���l�y��е� PVDF ���������L�Ļ���Ĺ��м�������(e) ��ͬ�l�y��е� PVDF 늌Wģ�M�Y����(f) �ΑB�� NG ��������õ� SEM �D�����ߣ�5 ��m���� 2 ��m���ң���(g) ��ͬ���DĤ�ĺ������əC�ơ�

�D 16 ���ڂ������ϵ� PENG�� (a) �ڃ�Դ늈������l�Ă������ϙC��ʾ��D��(b) 늼� P(VDF-TrFE) �{���w�S֧��ֲ�����Ƥ�´��ȅ^���ϣ��Ϳp�Ϻ�ֲ�벿λ���£��ĈD��(c) �gЪ����ֲ��֧�ܵ����ݔ����(d) L929 ���w�S�����ڼ��l�ĽM�����B�۱���ϩ����ֳ�ėl�ΈD��(e) �� Ag 늘O��� PZP ��ʾ��D���Ԝy���Cе�����a���ĉ��늉�������ܶȡ�(f) ͨ�^�Cе������ ZnO NR �ΌӮa���ĉ��늉��M�������� (g) Ƥ�¾��x�y���Ă��ڲ�λʾ��D��(h) С��Ƥ�w���ڵ���Ƭ�����Լ�ͨ�^�� PZP �ϸ��w����Ĥ���Ō� PZP �����ڂ����ϣ��ң���(i) �ί��� 0��3��7 �� 10 ��Ĵ�����Ƥ�w������Ƭ��

�D 17 ����ˎ��ݔ�͵� PENG�� (a) FeGa@P(VDF-TrFE)�˚��{��ʾ��D��(b) �ɗl�{���� AFM �D������ FeGa �� P(VDF-TrFE) �{�����L���ɡ������ߣ�200 nm��(c) ���к͛]�дň���¶�� FeGa@P(VDF-TrFE) �˚��{���@�õĉ��푑����ȭh��(d) �˚��{�����F�����D�ň��е��\��ʾ��D��(e) �ٿv�{������ѭ���K���Π�����ߣ�20 ��m��(f) �@ʾ����oˎ���ķ�����(g) ������ϼ{���c PDA ��ˎ��Ĺ��ܻ���Ȼ���Ǵ��|�lˎ��ጷŵķ�����(h) �ӕr�D���@ʾ���ڸ�׃�ň������r����ϼ{�����ı���������Ӿģʽ�D׃��[���\�ӡ������ߣ�15 ��m��(i) �@ʾ�ڲ�ͬ�����£��o PVDF���� P(VDF-HFP) ���� P(VDF-TrFE) �� NW ጷ� RhB �ĈD��

�D 18 �����o�������ί��� PENG�� (a) ���ڙC���W�����fԒ���R�eϵ�y�Ŀ��wʾ��D��(b) �ܻ���Ĥ���l�����ԉ���W��������ʾ��D��(c) �ܻ���Ĥ����Y�����l���� PMAS �ķ������l�����ƺ��Ƅ����������J�C��ʾ��D��(d) �Ķ�ͨ�����x����Z���l���Ϯa����������̖��ʾ��D��(e) ��ͨ�����ԉ���W������ӛ䛵Ę˜ʻ�Ů���Z��������̖����������̖�� (f) �A�ڃɂ� Ag NWs 늘O֮�g�������|�P���Ĕ��a��Ƭ�������ߣ�3 ���ס�(g) ���r���ώ��|��Ĥ�ľ��w�D����(h) �����|�P���Ķ̕r�����~׃�Q�l�V�D��
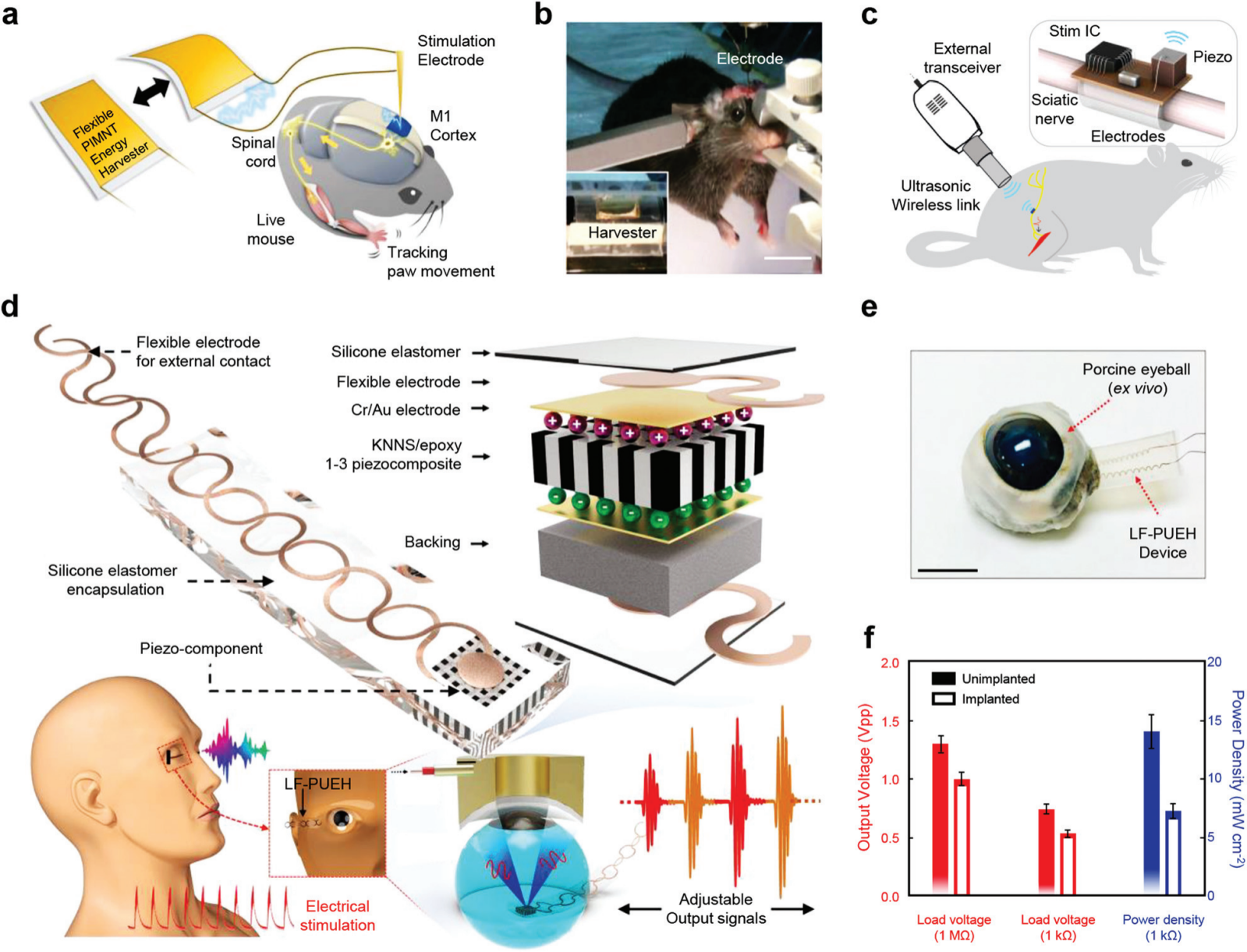
�D 19 �����̼��� PENG�� (a) ʹ���`��� PIMNT �ո�C��С���M���X�̼��Ą����f����(b) �B�ӵ��p�O�̼�늘O������ PIMNT �̼�������Ƭ��ԓ늘Oλ�� M1 Ƥ������늴̼��������ߣ�1 ���ס� (c) ���ڴ̼����������ğo늳�ֲ��ϵ�yʾ��D�� (d) ����ҕ�WĤ늴̼��ĺ������Գ��T���o�� PENG ��ʾ��D���OӋ��(e) ֲ���г�������O��Ĺ�W�D����ģ�Mֲ������� �����ߣ�1 ���ס�(f) ע��ͷ�ע����r������ݔ��늉������ܶȵı��^��
�D 20 �����t�����W�� PENG�� ԓ����ϵ�y���������܂����������ԙz�y���N������̖����ͨ�^ 5G �W�j�����N������̖�h���x�o����ݔ�o�t��������������ɺ��t������ͨ�^���ߵ��w�ȡ��w�ȽK�˺��O�����߷�������ָ���ί����Ķ����F�]�h�Ă��Ի��t��������
����朽ӣ�
Piezoelectric nanogenerators for personalized healthcare
W. Deng, Y. Zhou, A. Libanori, G. Chen, W. Yang, J. Chen, Chemical Society Reviews, 51, 3380-3435
https://doi.org/10.1039/D1CS00858G






















