�[�������h(hu��n)���c�[�����L���D(zhu��n)�ƺ͏�(f��)�l(f��)�������P(gu��n)��������[���ů����R��Ч�������]���R���[���ů���RT�����ߵ����w�����Ժ̈́�����ه�ĸ����ã����T��W(xu��)����·�F��O(sh��)Ӌ��һ�N�ɲ������[��(li��n)�ϲ��ԣ��Dһ������һ��ͨ�^�o��(chu��ng)�Ϳɿص͏����}�_����LIPUS���������̼������[���h(hu��n)������ˮƽ�������[���ů������ԡ��ڶ��������ý��ٶ�Ӽ{���f��ƽ�_���F(xi��n)�[���ů�������(li��n)�ϯ��������� PEG-���ż(li��n)�ů������K��Pt�������c�� PEG-purpurin 18��PEG-P18���M�b�ɼ{���w����NPs������ PP18-Pt NPs��ԓ�{���w���������õ����������Ժͻ��wˎ�������W(xu��)���ԣ���X-ray �� ����US���̼��£��Ɍ��F(xi��n)��ˮƽ�Ļ������錧(d��o)���[������������
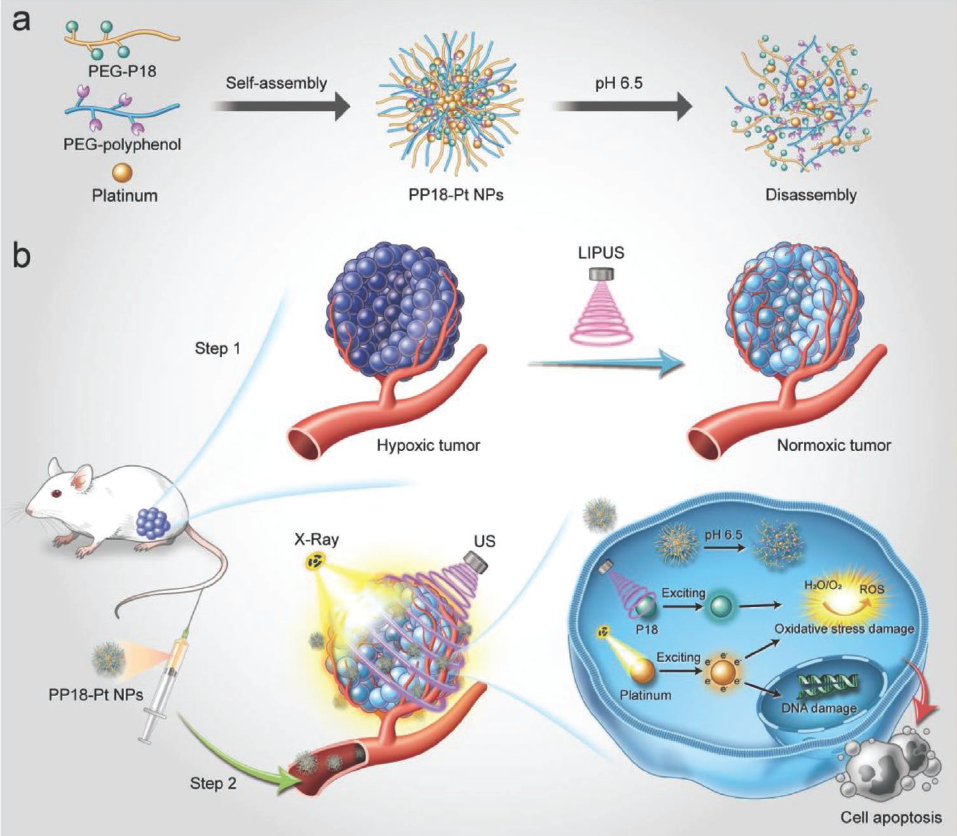
�Dһ�����ٶ�Ӽ{���w���Ę�(g��u)�����ί�����

�D�����͏����}�_����LIPUS���{(di��o)��(ji��)�[�������h(hu��n)����

�D�������ڽ��ٶ�Ӽ{���f��ƽ�_���[���ů�������(li��n)�ϯ����Ŀ��[��Ч��������(y��ng)�Ŀ��[�����ߑ�(y��ng)��
Փ����Ϣ��A Two-Step Flexible Ultrasound Strategy to Enhance the Tumor Radiotherapy via Metal�CPhenolic Network Nanoplatform. Adv. Funct. Mater. 2022, 2205690.
ԭ��朽ӣ�https://onlinelibrary.wiley.com/doi/full/10.1002/adfm.202205690
- ��ɽ��W(xu��)�Ƕ�ؔ/�S�ſ�/������/���x�F� Adv. Mater.�������L�v���ԵĿ�ע����̿�{��øˮ���z���F(xi��n)�[���ąf(xi��)ͬ�ί� 2025-07-04
- ���д����ڣ��w�� / �Ʊ��҈F� ACS Nano �����AIE�{���R�_ͻ���[������ - ���F(xi��n)���ʹ��\�� 2025-05-29
- ɽ�|��W(xu��)����ϼ���ڈF� Nat. Nanotech.���l(f��)�F(xi��n)��QCAR-T�����������w����Ч������Ч���� 2025-05-20
�\���P(gu��n)ע�߷��ӿƼ�

- ���ܹ��A��朆���������22��...
- �������C����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����츣��/��혡�������ǻ...
- ��ɽ��W(xu��)�Ƕ�ؔ/�S�ſ�/����...
- �Ї��r(n��ng)�I(y��)�ƌW(xu��)Ժ����о�����...
- ��������� Adv. Sci.: �ň�...
- ���t(y��)��ë��Fꠡ��������R��...
- ������/���ƴ�Ժ����ƽ...
- �B�T��W(xu��)�܌W(xu��)������ Macromo...
- ɽ���܂������ڡ������w�ɷ�...
- �A���r(n��ng)������p���ڡ�����x...
- �Ї��ƴ���Ƙ�/���������...
- �B�T��W(xu��)������ڈF� AFM��...