�^�i���[��������R�����Ҋ�İ��Y֮һ���������MչѸ�٣�60%���ϵIJ����l(f��)�F(xi��n)�r���������ڣ��������ڻ����У�����50%-60%�Ļ��ߕ����F(xi��n)�g(sh��)��Ͱl(f��)���D(zhu��n)�ƣ�����5���������^�͡����g(sh��)�г����J�����R���ί��^�i�[������Ҫ�ֶΡ��s40%-60%������HNSCC���������g(sh��)������F(xi��n)�ֲ��Ͱl(f��)����Ҏ(gu��)�����ͷů���(j��ng)�������A���g(sh��)���[���Ͱl(f��)��Ȼ�����@Щ���ܵ�ȫ�����ԡ���ˎ�Ժ�����ϵ�y(t��ng)�p�������ơ����գ��A�пƼ���W�����ƌW�c���g(sh��)�WԺ�����ڈF��c��h��W��ǻ�t(y��)�WԺ�O־܊���ڈF��Լ����w�S�أ�BC������ģ�������(g��u)����һ�N��ܵĿ�ֲ������������w�S��Ĥ�oˎģ�ͣ�TB/��PD-1@AuNCs/OBC����ԓ�о������������w�S��Ĥ�W(w��ng)�j(lu��)�Y(ji��)��(g��u)��ؓ�d��Ѫø�c��{�\���dPD-1���w��(y��ng)�����^�i�[���g(sh��)���ί�������Ч���T���[������������������ߙz���c����ί���푑�(y��ng)�ʣ������[���g(sh��)��ďͰl(f��)��
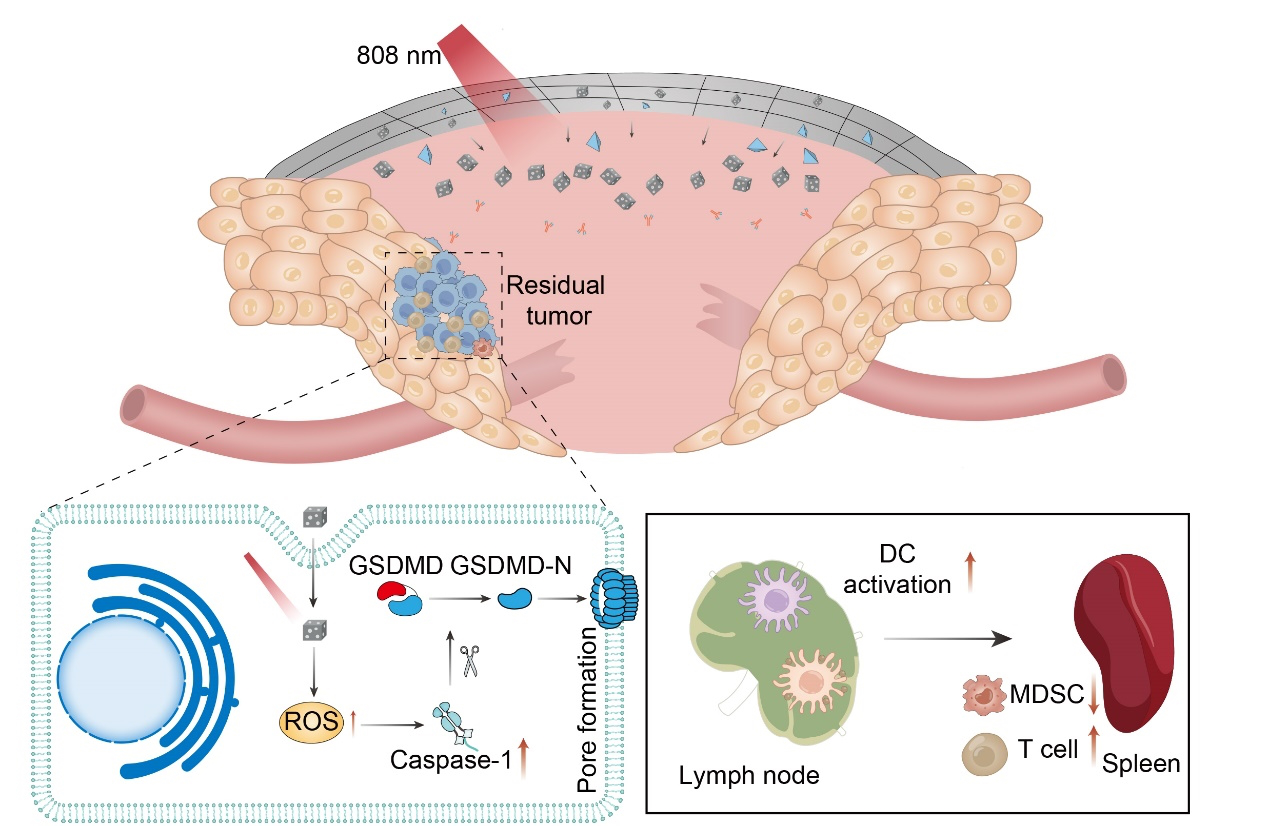
ԓ�oˎģ��ͨ�^��{�\�Ĺ��Ч�������[����λ�a(ch��n)����������ROS�����T���[����λ�ļ���������ጷ��[�����P(gu��n)��ԭ�����ԭ��ʼ������M������T�����錧�Ŀ��[�����ߡ��@��������ߙz���c����푑�(y��ng)�ʣ��Ķ������[�����L�Ͱl(f��)�����L��С������r�g��ԓ�oˎģ�;��Ѓ�(y��u)������ﰲȫ�ԣ�չ�F(xi��n)�����õ����t(y��)����Ч��(y��ng)���O�ѵ��R����(y��ng)��ǰ����
�D1.AgNCs ����R�D��TEM�� �c������R�D��FESEM����AuNCs ����R�D��TEM�� �c������R�D��FESEM��
���ڽ�{�\��AuNCs����(y��u)����ˎ���f�ͺ���D(zhu��n)��������ԓ�о��x��AuNCs��������Ҫ��ˎ���f���d�w����������ÓQ��ͨ�^AgNCs�Ƃ���ɡ��ĈD1����R�D�ɿ���AuNCs�����пն�ĽY(ji��)��(g��u)�����������Mһ��ؓ�d���ߙz���c���wPD-1�õ���PD-1@AuNCs��

�D2.ֲ��ʽ������������w�S��Ĥ��TB/��PD-1@AuNCs/OBC���Ƃ��^���в�ͬ���ֵ�FESEM�D��
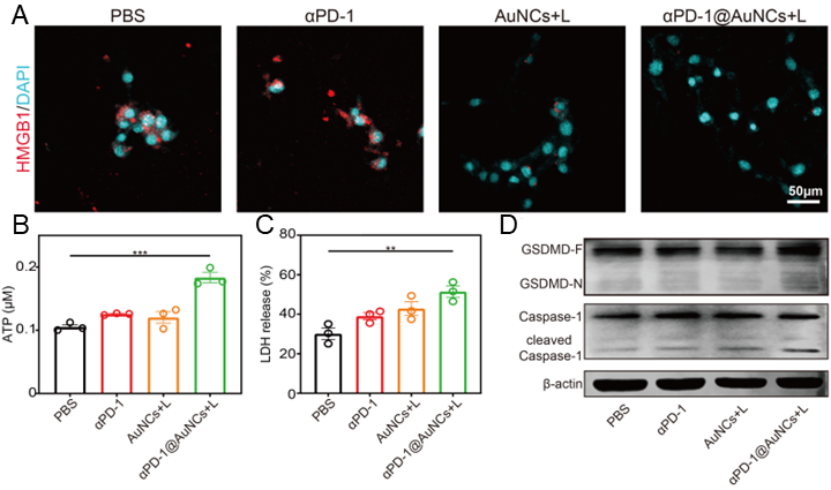
�D3.��PD-1@AuNCs���w�⌍��A����ͬ�ί���ጷ�HMGB1�ļ����ɹ⣻��B����ͬ�ί���ጷ�ATP����r����C����ͬ�ί���ጷ�LDH�ij̶ȣ���D����ͬ�ί����������P(gu��n)���ı��_��r��

�D4.��A���^�i�[��С���g(sh��)��ģ�͵��ί�ʾ��D����B����ͬ�ί���С����[���Ͱl(f��)�����L��������C����ͬ�ί���С���w�ص�׃����������D����ͬ�ί���С��������������E����ͬ�ί���С��Ļ��w����

�D5.��A����ͬ�ί�С���ܰͽY(ji��)�г����ͻ�����DCs���ı�����������������B����ͬ�ί�С��Ƣ�K��CD8+T�����ı�����������������C����ͬ�ί�С��Ƣ�K����Դ�����Ƽ�����MDSCs���ı���������������
���ԓ�о�������ʽ�����g(sh��)�z�y����Ҫ���������е��������P(gu��n)�����ĸ����̶ȡ�
��(j��ng)�^TB/��PD-1@AuNCs/OBC+L�ί��ɹ����M�ܰͽY(ji��)�е�DCs���죬������Ƣ�K��CD8+T�����Ľ�������������Դ�����Ƽ����Ĕ�(sh��)������Ч�خa(ch��n)���������[�����ߑ�(y��ng)��
ԓ�������A�пƼ���W�����ƌW�c���g(sh��)�WԺ�����ڈF��c��h��W��ǻ�t(y��)�WԺ�O־܊���ڈF꠹�ͬ������ɡ�Փ�Ĺ�ͬ��һ���ߞ��A�пƼ���W��Ժ���ʿ���F(xi��n)���Ϻ������}�о�����ʿ����h��W��ʿ���ܿ������A�пƼ���W������ڡ���h��W��ǻ�t(y��)�WԺ�O־܊���ڡ���h��W��ǻ�t(y��)�WԺ�����������ڞ�ԓ���µĹ�ͬͨӍ���ߡ�
Փ��朽ӣ�https://doi.org/10.1007/s12274-022-4811-7
- ����Ƽ���W����͢����W���P ACS Nano���������f(xi��)ͬ���á���(g��u)��������ˮ���z늽��|(zh��) 2025-04-17
- ���������F� CEJ�����ړ]�l(f��)���ЙC������z�y��ʯīϩ/����������/�����w�S��/���Ҷ����ͺϚ����z 2024-10-28
- ����������W��˼��n�}�M IJBM������������z�Ķ���x�輰��f(xi��)ͬ��(y��u)�� 2024-09-10
- �m��������WȽ�^���� Biomacromolecules����늾ۺ����Ƃ�M��ճ���Կ�ֲ�볬������� 2025-06-17
- ��������������/���D�����ڡ����Ϲ����S���۽��� Adv. Mater.: ��ֲ��ʽ�o��ˮ���z������������F(xi��n)�p����(j��ng)�{(di��o)�� 2025-04-24
- ֮��������R־܊�����AΣ�r��Adv. Mater.���������L�����������ԵĿ�ֲ������늘O - Һ�B(t��i)���������w�S���� 2025-01-15
- ���д����ڣ��w�� / �Ʊ��҈F� ACS Nano �����AIE�{���R�_ͻ���[������ - ���F(xi��n)���ʹ��\�� 2025-05-29
�\���P(gu��n)ע�߷��ӿƼ�

- �������C����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...