�������Ϸ��t�ƴ�W���������ڡ��Ϸ��t�ƴ�W�Ϸ��tԺѪ���c����ƺΕԷ����κ��w�|��ʿ���V�|�t�ƴ�W���ٵ�һ�tԺ�S�Ѻƽ�������ְl�]���A���R���Ľ����ںσ��ݣ����Һ�w�⻯��˨������ʹ������w��һ�Ӿ������õķ����ԣ�ͬ�r߀ʹҺ�w�⻯�;߂��˃����ĽY������׃�������@���������R��Һ�w�⻯��˨����˨��Ч�����о��ɹ��ԡ�Janus Particle-Engineered Structural Lipiodol Droplets for Arterial Embolization�����}�ھ��l����Nature communications�ϡ��Ϸ��t�ƴ�W�Tʿ�о�����˼�����Ϸ��tԺӰ����ֱ����t���鱾�Ĺ�ͬ��һ���ߣ��S�Ѻ����ڡ��w�|��ʿ�����������ڞ鱾�Ĺ�ͬͨӍ���ߡ�
��1978�꣬�ձ�����������WYamada������������܄��}����˨��(TACE)�����ԁ����Ե⻯�͞������Һ�w˨����������X���¿��@Ӱ���ܔy�d��N����ˎ�ȃ��c���яV���������R���[�����ش����ί���Ȼ�������^40�������R�����`���˂��l�FҺ�w�⻯��˨�����wϵ�ܲ�������˨�������������������Ѫ��ͨ��ͬ�r���⻯�ͽ�Ѫ��߀�������Ӳ����e�������M�����٣��M�����²������l�Y�Įa�������˨���ȷǰ���˨���ȡ�

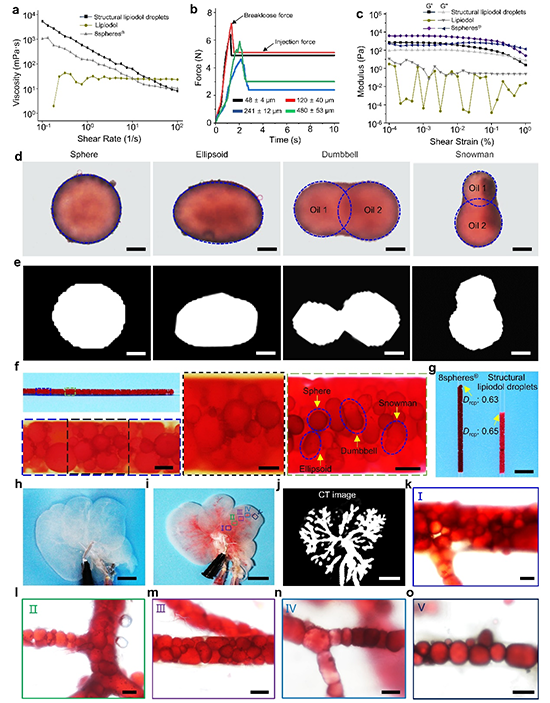
����Janus�w���ĽY�����⻯����Һ������Ѓ�����ճ������׃�������܉��m����ͬ�߶ȵ�Ѫ�ܽY����ͨ�^��׃���_�h�˸����Ą��}Ѫ�ܣ����F�h��Ѫ�ܽKĩ˨����

������R���⻯����Һ��˨������Janus�w���ĽY�����⻯����Һ����������õķ����Ժ��@Ӱ�������܉��L�r�g���e�ڄ��}Ѫ���У�չʾ��������˨��������
�����о��õ��ˇ�����Ȼ�ƌW����͏V�|ʡ���A�c���û��A�о���Ȼ�ƌW������Ŀ��֧�֡�
������Ϣ��
Sijian Tao, et al. Janus particle-engineered structural lipiodol droplets for arterial embolization. Nature communications. 2023, 14, 5575.
https://www.nature.com/articles/s41467-023-41322-6
- ���A��W�������n�}�M Macromolecules�����w�ܻ��c�����fͬ���Fһ偷��N����Һ�ۺ��Ƃ䲻ͬ��òJanus�w�� 2025-06-11
- ���A��W������/�����ҽ��ڈF� Adv. Mater.: ��Janus�w���{�ظ߷��ӏͺϲ��ϷӽY������ȡ���Mչ 2024-02-02
- ���A��W�������n�}�M Macromolecules: Janus�w���������п��Y���Ķ�����w 2023-08-14
- �A�ώ������M��Ϣ�����n�}�M��ACS Macro Lett.��������˨���� - UCST�Զ�λ�\ 2023-02-26
- ���A��W���o�����n�}�M��Һ�B���ُͺ�ʽ�[��˨�������� 2019-12-04
