�{����Դ��������о��T�F� Sci. Adv.������λ������Ŀɴ���ʽ���wܛ�M�����ӳ����g
�ڻ��w�ȳ���ܛ�M�����u���L������������B���Լ��黼�����������R�������Ϳ����A�����ش����x��Ŀǰ�������ķ���������g����Ź������MRI��Ӌ��C���Ӓ���CT���M���ڙz�y�����Ͼ��Ѓ��ݣ������O���w�e�����������ء��ɱ��߰����ܺ��^�ߵȷ�����ھ����ԡ��S�����r�z�y����IJ������ӣ���yʽ���p�������ɶ��ƵĿɴ������w�O�y���g�ܵ�Խ��Խ����Pע����ᘌ����K�����ٵij������O�䣬�Լ����B�ȳ�Ѫ���еĴŸБ����ӳ����g��Ȼ�����@Щ�O�������R�T����������|��ϸ��A��Ƥ�w��׃�������̖ʧ��Ȇ��} ������Ҫ���ǣ����ڽM���ɷֺ�������B�Ĺ��в���Hͨ�^һ�N�ɴ��������O���y�Ԍ��Fȫ��ľC�ϙz�y����ˣ����ڶ��ӻ�����C�ƵĿɴ��������O����аl��Ȼ�Ƿdz���Ҫ�ġ���迹���ӳ���EIT�������ؽ��ض��^���늌W���ԵĿ��g�ֲ���Ҳ�����������t�W�����һ�������о���֧���M��֮ǰ���о��ѽ���C���_ʽEIT�x�������w���ٱO�y�еĿ����ԣ����_�l���ڄӑB�M������Ŀɴ����ͱ�yʽEIT�O�������R���ɻ��A�����𣬰������Դ������l����ԡ��O��С�ͻ�����Ĵ��_�Լ��������Ч��������Ҫ���ǣ�������EIT�Ќ��F���|��������Ҫ����ע����������^�ȵ�����̼����ܕ���Ƥ�w�a������p������ˣ�EIT�ĈD���|����ه�ڵ����߱����Ӳ���OӋ������Ҫ���y�����Ƃ����Խؓ�d�m���Ժ���̖�|�������Դ��
���Q�@Щ���}�������{����Դ�cϵ�y�о���������о��T�F������һ�N�����v�O�wλ��������迹���ӳ���TIT���Ŀɴ������g�����������������e�ęz�y������F���wܛ�M���ij���z�y���@������Ħ���o늵ij������ݔ���߶ȿɿص��D��늺ɱ��|����ʹ�����܉���������N���Ѓ������������Ե���������O�䡣���@�N��r�£����o������c�迹���ӳ���ij����㷨��Y�ϣ����ܞ�ɴ������ӳ���ϵ�y�_��һ�N���صIJ��ԡ����������OӋ��һ�N���ڏͺ�Ħ�����Ч���ĸ߾����o���̖Դ��HESS������ԓTITϵ�y�ṩ����Խ���������Եĸ��|��̽�y���̖��ͬ�r����ʹ���h�����t���O�䰲ȫ�˜ʵ������̖���F�����迹������HESS�Ŀ��C��ʧ���_��0.03%�����׃���ʽ���0.01%���@�N��̖�|�������������Ħ����O���Џ�δ���F������ԓTITϵ�y������ˌ����w֫�wܛ�M���Ŀɴ����r������Ԍ��F�������\�Ӻ��\����D�ĄӑB�^�죬ͬ�rͨ�^TIT�O��@ȡ�ęM����D��߀�܉�^����ӽM���е�С������׃���������ۡ��{�胞�������������Ժ��p�����OӋ��ԓTIT�O����c�t���o������������ܷ��o�����ɣ����ڰ���ܛ�M���\�ӌW��������Ӳ�׃�O�y���������ί��ȶ��ӻ��đ��á�
���P�����ԡ�A wearable triboelectric impedance tomography system for noninvasive and dynamic imaging of biological tissues�����}�l���ڡ�Science Advances����DOI: 10.1126/sciadv.adr9139������ʿ�����i��Փ�ĵĵ�һ���ߣ�������о��T��ԓՓ�ĵ�ΨһͨӍ���ߣ�����Ԭ��÷����ָ����������Cе�Y�����OӋ��
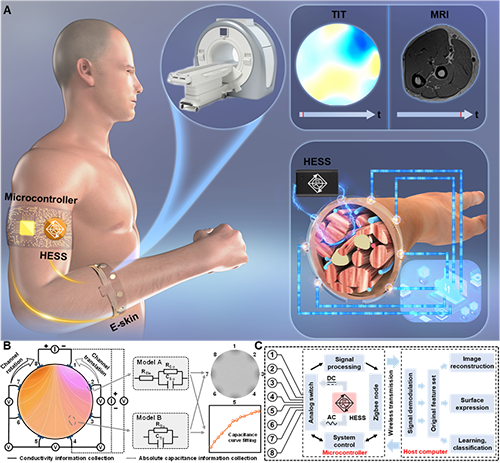
�D1��TITϵ�y���OӋ������ϵ�y�M��������
��D1��ʾ����Ӳ���Ƕȁ�����TITϵ�y��HESS��������̖���ɣ������Ƥ�w��e-skin������z�y�����������������ڔ���̎�����M�ɡ����Ƥ�w�ռ�ע��������迹������Ϣ������̎��ģ�K�ɿ������ɲ�ͬܛ�M���ĕr׃����ʈD��ᘌ����w�����Y�����Ƶ�����M���迹ģ�͌��ڈD���ؽ����P��Ҫ���迹�W�j�Ƀɂ������迹Ԫ����늘O-Ƥ�w��A���̓Ȳ��M����B����������B���γɡ������迹Ԫ��A��늘O-Ƥ�w����֮�g����裨RE-S������ݣ�CE-S�����Լ�늘O��裨REle������늘O�cƤ�w�Ľ��|�l���Q�����迹Ԫ��B��ʾ�Ȳ�ܛ�M�����迹�����нM���ڂ���λ�õ���裨RTis������ݣ�CTis���c�M����ͺ͠�B���P����ˣ��M������������׃������׃����늅���������ֲ��迹׃�����Ķ�ӳ�䵽߅��늉������˫@ȡ�������Ϣ��TITϵ�y�����Ķ˜y��ģʽ���x��ɂ�����늘O�������ע���c�������Ώ���������늘O���ռ�늉���̖��ͨ�^��׃���ע����ԣ������Ì���늘O���M��ֱ����DC��ע�룬߀���ԫ@�ð������w�M���^�����ֵ������������TITϵ�y�����w�OӋ�������ψD��ʾ������8��늘O���ɵ����Ƥ�w�ϣ���ͨ�^�����·�c���������B���ռ�����������Ϣ��Ҫ�����CӋ��C���M��̎�������F�D���ؽ������ڙC���W���ķ���ܡ�

�D2 E-skin��HESS���OӋ�����ͅ�������
���������w������̖ݔ���͔����ɼ������Ƥ�w��e-skin�������Čӹ��ܽY���������b�ӡ�֧�Όӡ���늾W�j��ճ���ӣ������С��10 ��m����늾W�j���ÈD�����OӋ���������|늘O������ݔ������Pedot:PSS-�۰�����PU��-�y�{����AgNWs��(PPPA)�Ƴɡ��������ӹ��܌ӄt�Ծ���ϩ��/�����ǣ�PVA/CS����Һ������A���ϡ�PVA/CS�c�iƤ֮�g�����쏊�ȡ����Џ��Ⱥͽ����g�Էքe��53.16 kPa��72.76 kPa��2.49 J·m?2���@�Nճ�������܉���500��犃��ṩ�ɿ��ĸ������ܡ����⣬ͨ�^���AgNWs���L���ȣ�PPPA��늌����@����ߡ����c�̘IAg/AgCl���z늘O��ȣ����Ƥ�w�����w�ϵĽ��|�迹�@�����ͣ��H�����z늘O�迹��35%��
HESS������105 g�����Џͺ�Ħ�����Դ�����ṩ�����Ҹ߶ȿɿص�̽�y�������ԓ�ͺ����Դ�У�ֱ��ģ�K�a����ݔ��늺ɲ��H���Ԫ���ݔ���Լ��������t���O�䣬߀�ɂ�ݔ������ģ�K���Ŵ�����Kݔ��������@�N늺�ע�뷽���˷��˂��y����Ħ���Դ푑��r�g�L�������Բ���ɔ_�����͵�ȱ�ݡ����⣬���о������һ�N�ӑBƽ����ԣ����ڶ�������HESS������ԡ�������DC��̖�ڎ����ȵļy��ϵ������5%����Ϳ��_0.63%���c���ø߉�ֱ���Դ��ȣ�����ͬ�~��늉��µļy��ϵ���H����57%��AC��̖�Ŀ��C��ʧ�����1.2%����̓H��0.03%�������ǻ�����������̖��Ӱ푿��Ժ��Բ�Ӌ��ݔ������ȸ���110 dB����ֵ���_120 dB����TITϵ�y�ĸ߾��șz�y�ṩ�ˏ������ı��ϡ�ͬ�r��AC��̖�ķ��l�V�@ʾ����20-200 Hz�����ȣ�������ȱ��F���^�����l����ه�ԣ��������ڸ����l���»����c�l�ʟo�P���@��Ч��Q��ϵ�y�����Դ�Ȳ��迹���l��푑����}���Mһ����ͨ�^����PTFE��ȁ��{��ݔ���迹�������w�迹�y������У�HESS�ăȲ��迹�ڎ����ȱ����Ƶ�50 M����PTFE��ȣ�50 ��m������ˣ���HESS�c���w�B�ӕr����ݔ�������׃���ʃH��0.02%��
�������߂�64�������ɼ�ͨ�����o���OӋ��5×5 cm��������34 g���ɼ����ĕr����̖ͨ�^Zigbee��ݔ�����C�M�Д���̎������ͬ�x���y�õ�늉��M�Еr�l����^����C���������y���Ŀɿ��ԡ���늌��ʈD���ؽ��У��x��һ����˹-ţ�D�������������ܣ��������˹��ͨ�V�����������t�����ӣ��_������߅��늉���늌��ʷֲ�Ψһ��Ӌ����p�p�����㷨�D���ؽ��е�ģ������Ӱ����Ӱ߅�粻�ʴ_������������SDF�㷨�cOGN�㷨�Y�ϣ��γ�SDF-OGN�㷨���cOGN������ȣ�SDF-OGN�㷨�ؽ���ģ�M�D���Π�߅���������ͬ�r��Ч���Ƃ�Ӱ������ָ�ˣ��������`�RMSE�����Y��������ָ����SSIM������ֵ����ȣ�PSNR�����D�����Pϵ����ICC�������@�������Mһ���C�����@һ�c��

�D3 TITϵ�y����֫�\�ӵĈD���ؽ��Լ�TITϵ�y�c�t���o��������ļ��ɡ�
�������w�Ȳ��M����������ͺͼ�����Һ�ֲ��@��Ӱ�����M����늌��ʣ��@�w�F��֬����0.021-0.033 S m?1����ѪҺ��0.52-0.83 S m?1�����X��Һ��1.79-1.81 S m?1���ȽM�����ض�늌����ϡ����⣬�ڲ�ͬ������B�£��M��늌��ʱ��F��������缡����oֹ��B�^�ɵ��տs��B�r늌��ʼs׃��10%���@Щ�ڜy���M�����ϵ�늌���׃����ͨ�^߅��늉�������TITϵ�y���M���ؽ�������B��׃�����ڌ�TITϵ�y����������M���y���r��ע�������l�ʱ�������100 Hz���ϡ�TITע�����w������ܶȃH��79.58-99.47 mA m?2���@������IEC-60601��GB-9706�t���O��˜�Ҏ���İ�ȫ����ֵ�����ֲ�����ȭ��B׃�������ʳָ�r��MRI�@ʾĴ�L��չ����ʾָ�켡�l���@���ļ���׃����ͬ�r�����M��Ҳ�l����С���ΑB׃�����@һ�F��ͬ����TIT�D�����w�F���tɫ��ʾ�M��늌��ʵ��½�����ӳ�˼����տs�����{ɫ�^��t����늌������ӣ����ܚw���ڼ�����ɻ�M��λ�ơ�MRI�cTITϵ�y���ʴ_��ӳ����Ҫ�����տs�ą^����Ǻ�Ä�ǵ��ΑB��λ��׃�����^Сδ�����ؽ��D���в��@�������ֲ���u���ʳָ����ָ���o��ָ�r���@��׃�����F����ָ������������Ѫ�ܽM���У���TIT�D���б��F�������^��늌��ʵ����ӣ�����ԓ�^�����P�M���ķ��ɡ��S��TIT�O�䱻���ɵ��t���o��������У�����C���m���ԡ��D3�@ʾ���b��TIT�O�������������Ƥ�w�N����ǰ�ۜyԇ�^��HESS�����������^���ɺ�ͨ�^���ٲ�ж�Y�����b��������ϡ���D�@ʾ���cTIT�O�伯�ɵ��������ϵ�y��ܺͿ���߉����������Ñ����缡�o�����ߣ��Lԇ�����֫�����r���c�����Π����P��׃���Լ������M�����ʽ��������ͨ�^TITϵ�y�R�e������TIT�D���c�������\����D�ļȶ��P��������������a���o���������������o��������ɸ��N������ͨ�^ؓ�d10.5 kg�Č���u����������������ܣ�������12�N���������е�һ�������酢�����������z�y���ֲ�ץ�Օr������������oֹ�������M��׃��δ���ṩ������Ϣ�A�y��һ���ֱۄ�����Ȼ�������ṩ�����ļ����늌����Mһ�����ͣ���ʹ���H��δ����������TITϵ�yͨ�^ܛ�M��׃��ӳ����\����D��ԓ��Ϣʹ������M�����Ӡ�B���Ķ��@���������P�M�����ڽ�����������o����֫�\���^���У�TITϵ�y���m���Ȳ��M����Ϣ�����������������u���Ñ����\����D�����漰12�N�������\�Ӕ�������80%����Ӗ�����������z���㷨�����ķ��������GA-BP���W�j��GA-BP�W�j����3�ӣ�ݔ���40����Ԫ���[�،�18����Ԫ��ݔ����12����Ԫ���D4F������12�N������Ӗ����GA-BPģ��ƽ���ʴ_�ʞ�97.58%�����F�����R�e���ȺͿ����Ք��ٶȡ����û���GA-BPģ�͵���������������������ɿ����ṩ�c��������Dһ�µ�����֧�֡�
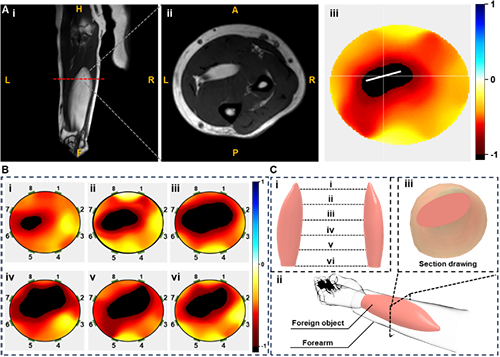
�D4 TITϵ�y�ؽ�ǰ��֬�����ĈD���u������Y����
�c���y�ɴ�����������ȣ�TITϵ�y���H�܉��R�e�����\�ӣ�߀�ܙz�y���ܛ�M���IJ�����׃����һλǰ��֬�������߅��c�˲����M���z�y�о���֬������Ҫ������֬���M���M�ɣ���늌����@����������ܛ�M�����ؽ��D���C����TITϵ�y���u��֬�����Ĵ��ڡ�λ�úͷ�����Ŀ����ԡ�TIT�ؽ��D���в�׃�^���Ժ�ɫ�@ʾ���Դ���MRI�^�쵽�ą^���@�w���ڞ�����TITϵ�y�ڲ�׃�z�y�еļ����Զ��x�����^�͵��ֵ�����⣬������־Ը���c���ߵ�ǰ���M��MRI��TIT�D����B�m���^�����u����ͬλ�õĈD�����ψDչʾ��TITϵ�y�ڲ�ͬλ���ؽ��ęM����D�����cλ�����P���·�13 cm̎���K�c�����P�������ψD�еĈD����֬����3Dģ�ͣ��cMRI������3Dģ����ȣ��w�e��H��5%���İ���֬�����ļ���ǰ��ģ�ͼ���M����D����Կ�����ԓģ�;��и߱���ȣ��M�㌦�����M���Ŀ�ҕ��Ҫ��
���о���B��һ�N�������wܛ�M�������TITϵ�y��ԓϵ�y��ه�ڌ����w�Ȳ�ͬܛ�M���Ϳ��Ƅ������wҺ���迹��Ϣ������ͨ�^�Y�ό��T���Ƶ��������͙C���W���������ؽ��㷨��Ŀ�˙M����ȵ��迹�ֲ��������ڌ��F����M���ğo�������Լ������M�����R�e�����|�����������ݵ������̖Դ��TITϵ�y�ĺ��ĽM�ɲ��֡����о������һ�N���������OӋ��ֱ��-�����Ŵ���Եďͺ����Դ���������̖Դ������Ħ���Դ��늙C�Ϳ����·�ڃȵ���̖Դ�����ɵ�һ���ߴ��9 cm×9 cm×2 cm��ģ�K�С��ڏͺ����Դ���£�ԓHESS�@����4-5 ��A��������ȣ����F���H��0.03%����С���C��ʧ����_120 dB�ķ�ֵ�������ע�����w������ܶȃH��79.58-99.47 mA*m?2��ݔ�������׃���H��0.02%���h����IEC-60601��GB-9706�t���O��˜�Ҏ���İ�ȫ����ֵ��
TITϵ�y�ڌ��H�yԇ�б��F��ƽ��SSNR��102 dB���Y�ϱ��о��_�l��SFD-OGN�㷨��TITϵ�y���F��1 mm/50 mm�����y�����g�ֱ��ʣ����@���˳���98.18%��ICCֵ0.9995�ĸ߱������Y�����ڴ���r�£�TITϵ�y���ԅ^�����P���܇���ǰ��������������С�z�y�Ƕȵ���3�㡣TITϵ�y�c�t���o��������ļ��Ɍ�������TIT�O���܉��Ч�R�e�Ñ����\����D��ƽ���R�e�����_95.4%���Ķ�ָ��������o��֫�w�\�ӡ����˼����\���⣬TIT�O��߀�ܙz�yܛ�M������Ӳ���׃����ͨ�^TITϵ�y����ǰ��֬�������迹��Ϣ���ɵ�3D��ģ�Y�����cMRI�Y����ȣ����w�e��H��5%���Y�Ͻ^����ݷ�����TITϵ�y߀���Կ������ǰ���]���ԓp�����۵ęz�y�΄ա����о������TITϵ�y�����˙C������������o���ί��������t�����I��ĸ��N�����ṩ��֧�֣�չ�F�ˏV韵đ���ǰ����
ԭ��朽ӣ�https://www.science.org/doi/10.1126/sciadv.adr9139




