�{��ˎ�ﴩ�ϰ������ġ��R�ס� ���ΰ�
2016-11-21 ��Դ���Ї��ۺ���W
ӛ����ǰ�ďV�|�t�ƴ�Wˎ�WԺ�@Ϥ,ԓ�WԺ��ʿ�������c�Ї��ƌWԺ�������M���g�о�Ժ�о��T���֝�����,��ͬԴ����{���dˎ��ҕ�������ί����Y����ȡ����ͻ��,�lչ�ˡ����ΰ������¯���,�о��ɹ������ڼ{���I��피��ڿ���ACS Nano���ϰl����
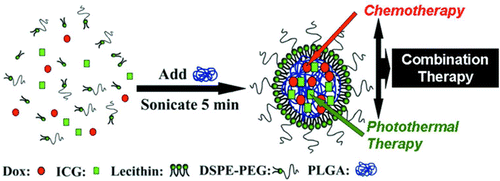 �������B,���о��Fꠘ����˰��d����ݼ�G(ICG)�ľۺ����������Ĥ�����{���w��(ICNPs),��������ͬԴMCF-7���ٰ��[�����\����ί���������Ĥ�ϱ��_��𤸽����,����Ƥ����𤸽���ӡ����}��ء�������������,ͨ�^���w�����w�Y����ʽ,�܉������˴������λ�������c���^�������{���w�����ϰ������ġ��R�ס��܉�𤸽�R�eMCF-7��������Ĥ��𤸽����,�����˷��ߵĻ��W������͝��ڵIJ��ɿ����ص�Ӱ푡�
�������B,���о��Fꠘ����˰��d����ݼ�G(ICG)�ľۺ����������Ĥ�����{���w��(ICNPs),��������ͬԴMCF-7���ٰ��[�����\����ί���������Ĥ�ϱ��_��𤸽����,����Ƥ����𤸽���ӡ����}��ء�������������,ͨ�^���w�����w�Y����ʽ,�܉������˴������λ�������c���^�������{���w�����ϰ������ġ��R�ס��܉�𤸽�R�eMCF-7��������Ĥ��𤸽����,�����˷��ߵĻ��W������͝��ڵIJ��ɿ����ص�Ӱ푡�
��������Ĥ������,�{���w�����H���b���Լ�,�p���˸��I�Ľ���,��K���F�ˌ�MCF-7�[����ͬԴ�������ڟɹ�/���pģ����������,���ý��t�⼤�⼤�l,���_�����[����λ�ľֲ��ض�,���F�˰��Y��ҕ�������ί������������f��
�������f,�{���w�������֬�IJ����ǰ�����Ĥ,�Ǐ��[���M���еİ���������ȡ������;�������w����ӵ�𤸽���Ӱ����R�e��������ͬ�N��ͬ�N��𤸽����,�Ķ����F���������\��,�ڼ�����l����,�{���w���Ĺ��a����������������;���Դ���[��,�������[��,���F�ˡ����ΰ�����
ԭ��朽ӣ�http://pubs.acs.org/doi/abs/10.1021/nn400334y

��������Ĥ������,�{���w�����H���b���Լ�,�p���˸��I�Ľ���,��K���F�ˌ�MCF-7�[����ͬԴ�������ڟɹ�/���pģ����������,���ý��t�⼤�⼤�l,���_�����[����λ�ľֲ��ض�,���F�˰��Y��ҕ�������ί������������f��
�������f,�{���w�������֬�IJ����ǰ�����Ĥ,�Ǐ��[���M���еİ���������ȡ������;�������w����ӵ�𤸽���Ӱ����R�e��������ͬ�N��ͬ�N��𤸽����,�Ķ����F���������\��,�ڼ�����l����,�{���w���Ĺ��a����������������;���Դ���[��,�������[��,���F�ˡ����ΰ�����
ԭ��朽ӣ�http://pubs.acs.org/doi/abs/10.1021/nn400334y
����c��؟�������W퓵ă������Ї��ۺ���W�ռ����W�ϰl������Ϣ�����@�á�Ŀ�����ڂ��f��Ϣ��������������ζ��ٝͬ���^�c���C�����挍�ԣ�Ҳ�������������h���H�ṩ����ƽ�_����������ؓ؟�����漰�֙࣬Ոϵ�҂����r�Ļ�h�����]�䣺info@polymer.cn��δ�����Wͬ�ⲻ��ȫ���D�d��ժ��������������ʽʹ��������Ʒ��
��؟�ξ���xu��
���P��
- �п�Ժ�{����Դ�������ՈF� JACS�����ЄӑB����λ�c��Ga/Zn�p��ԭ�Ӽ{��ø��߰��Y�ί� 2025-05-10
- ���_��W��־�ֽ����n�}�M Adv. Mater.: ԭλ����x�������������oĤ�������������Y���� 2025-05-08
- �|�ϴ�W�����۽��ڈF� CEJ �C�������������{�����ԵĹ��̻��z���ڰ��Y���װY�����������еđ��� 2025-04-09
- ɽ�|��W�������ڈF� ACS Nano: Ӳ�ȿ��{�ľ��Ҷ����{���w���{���{��-��������ã���������ˎ���f�� 2025-06-12
- �Ͽƴ��~�����n�}�M Nat. Commun.�����ߵ��x���w���Թ�W��̖�Ę������ӑB�{�� 2025-06-08
- �Ĵ���W������/�x溸��о��T�����B�����O���о��T AFM��һ�N����pH푑��Ժ�ܛ�ǝB�����ij����Ӽ{���w���ί����P���� 2025-04-30
