���������{���������Ҫ����֮һ���������������ؓ��������һ�����������ڙC�w��������ϵ�y�����ȍu�ط��ڼ����Ķ������ȍu�ع������㣬���������Ҫ�L���M���ȍu��ע���ί����ȍu��ֲ�ί����Է�������Ѫ��ˮƽ��ȥ���ȍu��ע����ه���p�������l�Y����δ�������ί�����Ҫ����֮һ��2004����ô�ġ��������D������ͨ�^�����w�ȍuע���벡�˸��T�o�}���ɹ����F���ȍu��ֲ��ʹ����Ó�x�ȍu��ע���ί����_����һ�������ȍu����ί����Ⱥӡ�Ȼ��Ŀǰ���ȍu��ֲ������Ȼ���R����ѪҺ�������ȍu����ʵ��Լ��ȍu�����L�ڹ��ܜp���Ȇ��}���������о���������Pע��ν����µ��ȍu��ֲ���g�ͷ�����
Ŀǰ�����WԺ�����t�W����ϵ�_���n�}�M�����Ե��_�l��һ��ڼ{��늼��z���ϡ�������нY�����ȍu֧�ܲ��ϣ��������ԓ֧�ܲ�����С��������ģ����֧���ȍu���g���|�ɼ�����ֲ�ί����Ĺ��ܡ����о��ɹ�Ŀǰ�ھ��l�����ڿ�Advanced Materials�ϡ�����еIJ����Ƃ��^����Ҫ�Y����늼������ͼӹ����g���@���˼����߶Ⱦ�������нY�������ڼ{�׳߶Ⱦ����w�S�Y���Ϳɿ��|���ܵĶ��֧�ܡ�����ԓ֧�ܲ��ϣ��ȍu���g���|�ɼ����γɵ��M�����Ա�����������֧�ܲ����ϡ����b�d���ȍu���g���|������֧����ֲ��һ������С��ģ���еĸ��G֬���|���ȍu���g���|�����@��Ѫ�ܻ�����ͨ�^�ȍu�ط��ڻ���M�����ޏ��_���ί�����Ч����
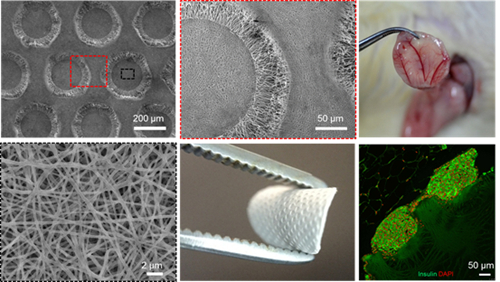
�о��F��uՓ�f�����������Y����֧�ܲ��Ͽ����ڿ��g������M�b��������ֹ�������������������h����ͬ�r�۰����{��늼��z���^�������W���|���ɲ����Ժã������˷�ˮ���z��Ŀǰ�����������W�ͼӹ��������Ć��}�����ڴ�֮ǰ���_���F�Ҳ����˾۰����ļ{��늼��z���Ͽ������ڼӹ����߸��x�b�ò����Ѓ�Խ�����������ԡ����P�о��Ѱl�����ڿ�Biomaterials��
�����Ŀ��g��λ�Ͷ��Ӽ��M�b�������������P�I���E֮һ�����֧�ܲ������ڽM�b�ȍu���M��չʾ��ͨ�^�������������㡱���ٵĸ����������һ�����ܲ�֧�ܲ��ϼ������µļ�����ֲ���g�춨�˻��A��ԓ헹�����Ҫ���c�ˆT���������t�W����ϵ��ʿ�о������P�������_���Tʿ�о�������ȡ�
