�����|(zh��)���z���䃞(y��u)�������������ԡ�����ɽ������Լ�ԭ�ρ�(l��i)Դ�S���������(l��i)�ڶ�N��(y��ng)���I(l��ng)��չ�F(xi��n)���V�ǰ����Ȼ�������y(t��ng)�����|(zh��)���z�ձ���ڏ�(qi��ng)�ȡ����ȼ��g�Բ���Ć�(w��n)�}������ҪԴ�����z�W(w��ng)�j(lu��)�д��ڵĴ�����Ҏ(gu��)�܄�ͨ����(hu��)������(li��n)�W(w��ng)�j(lu��)�Y(ji��)��(g��u)����˷��@һ���ƣ����������һ�N���Ͳ��ԣ������ú��п��{(di��o)���I���w��HBD��������܄���DES�������ɢ���|(zh��)����(g��u)�����иߏ�(qi��ng)�ȡ��߄��Ⱥ̓�(y��u)���g�Եĵ����|(zh��)���z��ԓDES�wϵ���H����(qi��ng)�˵����|(zh��)��g������ã�ͬ�r(sh��)ͨ�^(gu��)�����|(zh��)��c�܄�֮�g�ķǹ��r(ji��)���ã��ڷ����g��(g��u)�����S�������{(di��o)�Ľ�(li��n)�W(w��ng)�j(lu��)�������P(gu��n)�I���ǣ��@Щ��(li��n)�Y(ji��)��(g��u)��ͨ�^(gu��)�{(di��o)��HBD�(l��i)���M(j��n)һ����(y��u)�����Ķ���(sh��)�F(xi��n)��(du��)���z�g�Եľ���(zh��n)�{(di��o)��(ji��)�����ڵ����-朼������-�܄��f(xi��)ͬ���ã����õ��������z�����W(xu��)���ܷ�����F(xi��n)���@����(y��u)��(sh��)�������쏊(qi��ng)�Ȟ�10.25��1.28 MPa�����쑪(y��ng)׃�_(d��)892.51��39.66%������ģ����24.57��0.27 MPa���g�Ԟ�17.34��0.46 MJ·m-3�������ܞ�6.76��0.99 kJ·m-2������(y��u)��Ŀǰ���Ј�(b��o)���ĵ����|(zh��)�����z���ϡ�ֵ��ע����ǣ������W(xu��)���ܴ��������ͬ�r(sh��)��ԓ�(l��i)���z�Ծ��Ѓ�(y��u)����ճ���ԡ��ɻ����ԡ��h(hu��n)���������Լ���ȫ�ɽ����Եȶ�N�������ԡ����о������һ�N��(g��u)����߸��g���c����Եĵ����|(zh��)���z���²��ԣ������ڌ�(du��)���W(xu��)���ܺ����������p�������ǰ�ؼ��g(sh��)�I(l��ng)���еđ�(y��ng)���ṩ����Ҫ֧�Ρ����µ�һ���ߞ����Ʒ�������ͨӍ���ߞ���־�x�����ڡ����w�����ڡ��R�������ڣ�����ͨӍ��λ����ɽ��W(xu��)�h(hu��n)���c���W(xu��)���̌W(xu��)Ժ�����ݴ�W(xu��)��ɼ����У��
�����|(zh��)���z���䃞(y��u)�������������ԡ��ɽ����Լ��ɳ��m(x��)�ԣ��ڽM�����̡�������Ӻ�ܛ�C(j��)�����I(l��ng)������P(gu��n)ע��Ȼ�������y(t��ng)�����|(zh��)���zͨ������ɢ�Ćν�(li��n)�W(w��ng)�j(lu��)��(g��u)�ɣ���(d��o)����C(j��)е�������C���F(xi��n)��͏�(qi��ng)�ȡ��̈́��Ⱥ͵��g�ԣ��y�ԝM(m��n)���(f��)�sؓ(f��)�d��(ch��ng)���������⣬�h(hu��n)����(w��n)���ԣ��翹���ԣ����������Ժ�ճ���Ե����ܵ�ȱʧ���M(j��n)һ���������䌍(sh��)�H��(y��ng)����������ˣ��_(k��i)�l(f��)�C(j��)е��(qi��ng)�ȸߡ�Ӳ�ȸߡ��g�ԏ�(qi��ng)����ܵĵ����|(zh��)���z���P(gu��n)��Ҫ�������о�ͨ�^(gu��)�{(di��o)�ص�����g�ķǹ��r(ji��)����ã��ژ�(g��u)���ߏ�(qi��ng)�ȵ������z����ȡ����һ�����M(j��n)չ��Ȼ�����@Щ��(b��o)���ĵ����|(zh��)���z���F(xi��n)�����ęC(j��)е�C(j��)е������ߣ�����ģ��<0.5MPa�����쏊(qi��ng)��<5MPa��������<1kJ m?2�����@����?y��n)��܄������ɢ���|(zh��)�ڵ����|(zh��)���z�wϵ��ռ��(j��)�^���w�e��?j��n)?sh��)��ͨ������ҕ����ҕ��ͨ�^(gu��)��K�����|(zh��)��g����ö��������z���W(xu��)���ܵ����O���ء����y(t��ng)�܄�����ͨ�^(gu��)�c�����|(zh��)��γɸ�(j��ng)��(zh��ng)������ã�ʹ��g���x�����M(j��n)���������z�W(w��ng)�j(lu��)�Y(ji��)��(g��u)�ķ�(w��n)���ԡ�ͬ�r(sh��)�����z�W(w��ng)�j(lu��)����Ч��(li��n)�c(di��n)��(sh��)�����ޣ��M(j��n)һ�������˵����|(zh��)���zͬ�r(sh��)��(sh��)�F(xi��n)�ߏ�(qi��ng)�ȡ��߄����c���g�Ե��������b���܄��ڵ����|(zh��)���z����ռ�����������O(sh��)Ӌ(j��)ʹ�܄�����ͨ�^(gu��)�c�����|(zh��)�֮�g���خ��Էǹ��r(ji��)����ã��B����ͬ�����|(zh��)朶Σ���(g��u)����(w��n)���ҿ��{(di��o)�Ľ�(li��n)�Y(ji��)��(g��u)���������@������(qi��ng)���z�����W(xu��)���ܣ��Ķ�ͻ�Ƃ��y(t��ng)�����|(zh��)���z�����W(xu��)���ܷ����ƿ�i��
������l(f��)�c(di��n)��
(1)ͨ�^(gu��)���뺬���{(di��o)���I���w��HBD��������܄���DES�������ɢ���|(zh��)��ͬ�r(sh��)����(qi��ng)������g��(li��n)����ú������܄���(li��n)�����|(zh��)朣��Ķ��O������(qi��ng)���z�W(w��ng)�j(lu��)��(li��n)�ܶȣ��о��܄��������g���|(zh��)��(du��)�������z��(li��n)�Y(ji��)��(g��u)��׃��Ӱ���
(2)���ڵ����-朄�����-��܄��ąf(xi��)ͬ���ã�Ԕ��(x��)�о���C(j��)е���ܵ�����(qi��ng)���g�C(j��)�ƣ����쏊(qi��ng)�ȡ����ԡ��g�ԡ������g�Լ��Y(ji��)��(g��u)��(w��n)�����ԣ����M(j��n)һ���о����п��{(di��o)���I���w��HBD��������܄���DES����(du��)���W(xu��)���ܵ��{(di��o)��Ҏ(gu��)�ɡ�
(3)���ڪ�(d��)�صĽ�(li��n)�Y(ji��)��(g��u)���wϵ���о���ӡ�C�����z�������z�Ķ���ԣ��������������������Ϳ���ȫ���������������(y��n)�C�䌍(sh��)�H��(y��ng)�Ý������u(p��ng)���������������ɴ���������������늘O�����ز��ϵ�������
�����܄��ÓQ�����D1���������zˮ���z��������܄������Ȼ�đ�A-���ͣ�������܄�����ȫ�ÓQ����(g��u)�������z�������z��ͨ�^(gu��)�{(di��o)��DES�К��I���w��HBD���Ķ��u���Y(ji��)��(g��u)�����Ҷ������͡�ľ�Ǵ���ɽ�洼�����܄����Ӳ��H��������(qi��ng)�����|(zh��)��g���ã�ͬ�r(sh��)������"���Ә�"�B�Ӳ�ͬ�����z朣��γ����z�-�܄���(li��n)�������������zչ�F(xi��n)����(y��u)���������c���d������

�D1.�����|(zh��)���z�����z�������z�����Ƃ�
ͨ�^(gu��)�Y(ji��)��(g��u)������ʾ����������(qi��ng)�ķ��әC(j��)�ƣ��D2���� SEM�����P(gu��n)EDS�D�V������ľW(w��ng)�j(lu��)�Y(ji��)��(g��u)��DES�M�֣�����Ԫ�أ�����Ƕ�����z�W(w��ng)�j(lu��)��FT-IR��Raman���V�C��(sh��)�C�������܄������벢�c���z��γɚ��I��ͬ�r(sh��)��ʹ�����z��g����������(qi��ng)�����˸�������˽����z�������z���γ��^(gu��)�̣��M(j��n)���˲�ͬ���ݕr(sh��)�g�����z�������z������׃����FT-IR���V�������Y(ji��)���������z���z�аl(f��)���˿��ٵ��܄�����U(ku��)ɢ�����zÓˮ�����z�֮�g���I��(qi��ng)�������ҹ����܄��c���z֮�g�γ��������I��������Ҫ���ǣ�����ͨ�^(gu��)HBD�u����(sh��)�����{(di��o)�����z�-�܄���(li��n)�����C��(d��ng)HBD���Ҷ����D(zhu��n)׃��ɽ�洼�r(sh��)�����I��(li��n)�ܶ��@�����������z�W(w��ng)�j(lu��)��څ���ܡ�
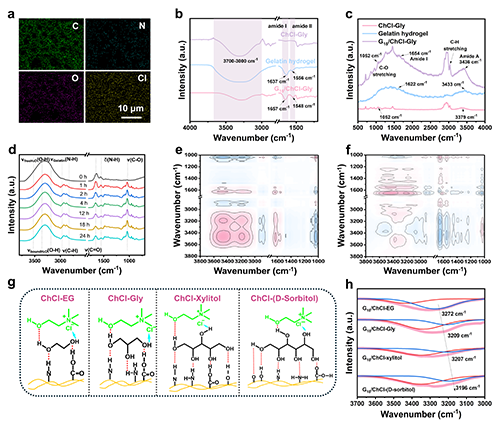
�D2.���z�������z�ı������������g�C(j��)��
�@�N��(d��)�ص����z�-朼����z�-���ׅf(xi��)ͬ������Ч�������ˮ���z�����W(xu��)�������D3�������z������10 wt%����20wt%�r(sh��)�����쏊(qi��ng)����1.33 MPa�����10.25 MPa������ģ����0.11 MPa ������ 24.57 MPa��ͬ�r(sh��)��ͨ�^(gu��)�{(di��o)��HBD��(du��)���z���W(xu��)�����M(j��n)����Ч�{(di��o)�أ�����G15/ChCl-��D-Sorbitol�����z�քe���F(xi��n)��6.34 �� 0.76 MPa�����쏊(qi��ng)�Ⱥ�3.49 �� 0.35 MPa�ď���ģ�����Լ�����15.51 �� 1.18 MJ·m-3�ĸ��g�Ժ�499.00 %�����쑪(y��ng)׃����֮��ͨ�^(gu��)��׃DES�е�HBD�����z�����������ںܴ���(n��i)��(ji��n)�εض������z�������z�ęC(j��)е���ܣ��������쏊(qi��ng)��0.53 �� 0.02��10.25 �� 1.28 MPa������ģ��0.073 �� 0.002��24.57 �� 0.27 MPa�����쑪(y��ng)׃��200.80 �� 44.88��892.51 �� 39.66%���g�ԏ�1.08 �� 0.12��17.34 �� 0.46 MJ·m-3���c���ڈ�(b��o)���Ĵ����Ե����|(zh��)�����z��ȣ����о�����(g��u)�������z�����쏊(qi��ng)�Ⱥ͏���ģ��������F(xi��n)���@���������������h(yu��n)���F(xi��n)���īI(xi��n)���ш�(b��o)���ĵ����|(zh��)�����z���ϡ����⣬ѭ�h(hu��n)���쌍(sh��)�(y��n)�(y��n)�C�����z�W(w��ng)�j(lu��)�Y(ji��)��(g��u)�Ŀ����ԡ���(j��ng)�^(gu��)10��50%��(y��ng)׃ѭ�h(hu��n)��(y��ng)���������Ը��_(d��)94.38%��������ʹ�ڲ��ֽ�(li��n)�c(di��n)��Ɖĵ���r�£����z�W(w��ng)�j(lu��)�Ծ������õĽY(ji��)��(g��u)��(w��n)�����c��(y��u)���Ŀɻ֏�(f��)���ܡ�

�D3. ���z�������z�Ŀ��{(di��o)��(ji��)�C(j��)е����
����ͻ�����ǣ����z�������z���Ѓ�(y��u)�������������ܣ��D4�������z��Ʒ˺�����ɸ��_(d��)��3.94 �� 0.50 kJ·m-2����1mmȱ�ڵĘ�Ʒ��������400%��(y��ng)׃���o(w��)�Ѽy�U(ku��)չ�������ܸ��_(d��)6.46 kJ·m-2�����y(t��ng)���zˮ���z�H1.65 J·m-2����ͬ�r(sh��)ȱ��ԇ������(j��ng)�v100��100%��(y��ng)׃ѭ�h(hu��n)���ԟo(w��)���@��(y��ng)��˥�p���D4f-g�����@�����ڳ��ز����I(l��ng)��đ�(y��ng)�Ý�����

�D4. ���z�������z�Ŀ��Ѽy�U(ku��)չ�����c��ƣ����
���⣬��ȫ������(li��n)�����z�������z���ж��ع����������D5�������ȣ�ԓ���z���Ѓ�(y��u)����𤸽���ԣ���(du��)PET���������~�Ȼ��ĵ���N���ľ����F(xi��n)����(qi��ng)��𤸽�ҿ��؏�(f��)���_(d��)10�Οo(w��)���@ճ����(qi��ng)��˥�p�����z��ճ�ԏ�(qi��ng)�ȿ�ͨ�^(gu��)�{(di��o)��HBD��17-93 kPa������(n��i)�M(j��n)���{(di��o)��(ji��)��ͬ�r(sh��)������܄��Ĵ����x��ԓ���z���õĭh(hu��n)����(w��n)���ԣ���-40���O���h(hu��n)�����Ա���535%���L(zh��ng)�ʣ����������ط���30���������������F(xi��n)��(y��u)����ԓ���z߀��ͨ�^(gu��)�ӟ�Ɍ�(sh��)�F(xi��n)���������ã������������Ա���600%�ĸ����쑪(y��ng)׃�ͼs3MPa�Ŀ�����(qi��ng)�������⣬ԓ���z����ȫ���⣬ˮ��72С�r(sh��)���������_(d��)94.78%������ƽ�����W(xu��)��(qi��ng)���c�ɳ��m(x��)�ԡ�

�D5. ���z�������z��ճ�������c�ɻ�������
�����u(p��ng)�����Ƃ����z�������z�Č�(sh��)�H��(y��ng)�Ý������D6���������������ͻ����z���z��������늘O�ɹ����@�߾��������̖(h��o)��PQRST��������������������Ag/AgCl늘O��ͬ�r(sh��)���鑪(y��ng)׃����������������ڲ�ͬ��λӛ��\(y��n)��(d��ng)��̖(h��o)�����ԫ@�������ҷ�(w��n)���Ă�����̖(h��o)����ɽ�洼�����z���z����ܛ�����"����"�����ɹ�����100g���w18 cm�������w�_�����C�������ڳ��ز����I(l��ng)��đ�(y��ng)�Ý�����

�D6.���z�������z�đ�(y��ng)����ʾ��
�C�����������о�������܄���DES�����ɢ���|(zh��)�����ú�(ji��n)�ε��܄��ÓQ���ԣ��ɹ���(g��u)����һ�N�������z�ď�(qi��ng)�g�����õĵ����|(zh��)���z�������z�������z����ͨ�^(gu��)ʹ��DES���ˮ���܄����@������(qi��ng)�����z�����֮�g������ã�������g�γɴ������z�-�܄���(li��n)�Y(ji��)��(g��u)���Ķ��x�����z��(y��u)�������W(xu��)���ܣ������ߏ�(qi��ng)�ȡ��߄��ȡ���(y��u)�����g�ԡ���ɫ�������ԺͿ��Ѽy���������⣬ͨ�^(gu��)�{(di��o)��(ji��)��Ԫ���(l��i)���I���w��HBDs���ķN�(l��i)������Ч�{(di��o)�����z��cDES֮�g�Ě��I���ã���(sh��)�F(xi��n)��(du��)���z���W(xu��)���ܵĶ��ơ��������@�N����Ľ�(li��n)�W(w��ng)�j(lu��)�Y(ji��)��(g��u)�����z�������z߀���F(xi��n)����N�������ԣ������õ�ճ���ԡ��ɻ����ԡ������Լ��ɽ����ԡ�������(y��ng)���о�������ԓ�(l��i)����ҽY(ji��)��(g��u)��(ji��n)�̵����z�������z�ڿɴ����������о������õ��m���ԣ��܉��`��푑�(y��ng)С�����ҵ�������(d��ng)��̖(h��o)��ͬ�r(sh��)��Ҳչ�F(xi��n)��������ܛ�w�C(j��)����ϵ�y(t��ng)�г��ؽY(ji��)��(g��u)�����ĝ�����ԓ�о����Ƃ��߸��g�ԡ���(qi��ng)���c����Եĵ����|(zh��)�����z�ṩ��һ�l����·������������Ҫ���ƻ��C(j��)е�c�Y(ji��)��(g��u)���Ե����M(j��n)���g(sh��)�I(l��ng)���еļ��ɑ�(y��ng)�õ춨����Ҫ���A(ch��)��
��ԭ����Ϣ��
Y. Li, Z. Qin, P. He, M. Si, L. Zhu, N. Li, X. Shi, G. Hao, T. Jiao, X. He, Fully Degradable Protein Gels with Superior Mechanical Properties and Durability: Regulation of Hydrogen Bond Donors. Adv. Mater. 2025, 2506577.
https://doi.org/10.1002/adma.202506577
- �пƴ���Ƙ�(l��)���ڈF(tu��n)�(du��) Angew��ͨ�^(gu��)�p�M�ִ����Ƃ�O�Ը߿��_�۱�ϩ 2024-11-07
- �F�ݴ�W(xu��)�x�������ڡ��x�h(yu��n)�i��Ƹ���ڈF(tu��n)�(du��) AFM���������Կɳ��m(x��)�ЙC(j��)��������������Ի��� 2024-03-17
- �Ϻ������ވF(tu��n)�(du��) CEJ�����Ѓ�(y��u)���C(j��)е���ܵğo(w��)��(y��ng)���p���Π�ӛ���ۺ��� 2023-06-23
- NTU�ğj/���A��W(xu��)���A��/�㽭��W(xu��)����� Sci. Adv.����׃�W(xu��)��ʽ��ʾ�L(zh��ng)��ճ���;��Եă�(n��i)�ڙC(j��)�� 2025-03-19
- ����W(xu��)�~�����ڵ� EES���������g�²��ԅf(xi��)ͬ�����ЙC(j��)���늳ص�Ч�ʡ���(w��n)���ԡ������������ԡ��C(j��)е�;��Ժ�ݔ������ 2025-02-13
- ������������С���о��T�F(tu��n)�(du��) Mater. Horiz.���ߜ��|�l(f��)��(li��n)���������ЙC(j��)��׃��(f��)�ϲ�������ȼ 2024-08-28
- ���A��W(xu��)�����n�}�M ACS Nano���ɞ����ˎ�﹩�ܵ���ȫ�ɽ����\늳� 2023-03-15
�\(ch��ng)���P(gu��n)ע�߷��ӿƼ�

- ����(b��o)���C(j��)��(hu��)��500+ˎ��...
- ��(gu��)�HƷ�ơ�ǰ�ؕ�(hu��)�h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ��(gu��)�a(ch��n)������٣����(gu��)���^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��(hu��)
- �Ј�(ch��ng)��300�|��PMEC China ɫ...
- ����ע��(c��)��2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �Ї�(gu��)�ƴ����(sh��)�����/é�|��...
- UCLA�R����/��ɽ��W(xu��)��־�x...
- �|�A��W(xu��)������/���ڈF(tu��n)�(du��) AC...
- ������W(xu��)��Ԫ����Adv. Mater...
- ������κ�/������ Small ...
- �|�A��W(xu��)�����/ʷ���(y��ng)��...
- �A�ƴ�Ǻ��� Sci. Adv.����...
- �칤��܊/���r�F(tu��n)�(du��) AFM...
- ���ϴ�W(xu��)Ƥ�������� Angew��...
- �Ĵ���W(xu��)�~�ֽ��ڈF(tu��n)�(du��) Small...
- ���A������W(xu��)�����n�}�M CEJ...