���ٰ���Ů���Y���P(gu��n)�����ʵڶ��ߵļ��������ί��漰���g(sh��)���ů����������o���ί��ȶ�N���ԡ�Ŀǰ���ί��������������ٰ����߷dz���Ч���������ں�/���D(zhu��n)�ƻ��ߣ����ڰ��Y��(x��)������ͨ�^���N�C���ӱ�����ϵ�y(t��ng)��������ã���(d��o)���[���Ŀ������L�Ͱ��D(zhu��n)�ƣ��ί�Ч���������˝M�⡣
�ӱ����߹����ǰ��Y��(bi��o)־�ԙC��֮һ�������ί����ڿ��Լ������������ϵ�y(t��ng)�Թ������Y��(x��)�������ί������������Y���²��ԡ�������(x��)���������������w��PD-1���������ί������������(x��)���ϵ�PD-1�c����(x��)���ϵ�PD-L1�ĽY(ji��)�ϣ��Ķ��錧(d��o)�[����(x��)���������ѱ���(y��ng)���ں�ɫ��������С��(x��)���ΰ���������ܰ������^�i�[���ȵ������ί���������߿��w�����ʡ�Ȼ�����ڌ��w�����������Ե��[���h(hu��n)���������ί��ڌ��w���еį�Ч�������˝M�⡣ͬ�r���������M����Ҳ���_(d��)PD-1��ʹ�������ί����ܴ����^��ĸ����á�
��������x��׃Ҳ���J(r��n)�����{(di��o)�ذ��Y���P(gu��n)�I���أ�ͬ�rҲ���[���D(zhu��n)������Ҫԭ��֮һ�����Y��(x��)�����ǽͽ��ƫ���ǰ��Y�M(j��n)չ���P(gu��n)�I���E���o���l���µ��ǽͽ�鰩�Y��(x��)���ṩ�˴�������ͬ�r���ǽͽ��^���Юa(ch��n)���������h(hu��n)�����Դ��M(j��n)�[���Đ������u���D(zhu��n)�ƺ��������ݡ�ͨ�^�{(di��o)�������ǽͽ�Ķ��{(di��o)�ذ���(x��)�����x�Ͱ��D(zhu��n)��, ��˳ɞ��˰��Y�ί��ğ��TԒ�}�����ἡ����ه�Ե���ø-1��PDK1����ͨ�^���Ʊ�ͪ��Ó��ø�������{(di��o)���ǽͽ⣬�Ķ��������ٰ��D(zhu��n)��, �����ٰ��ί���һ����ϣ���İ��c��
Ŀǰ�İ��Y�ί���ͨ�^�����������ݻ��ǽͽ��T��(d��o)�������h(hu��n)������ȱ��ᘌ����ߵ��p�ع��ܻ��ί��ֶΡ�����_�l(f��)��һ�N����ͬ�r�����������ݺ��{(di��o)���ǽͽ�������ί��ֶΌ����Ը��ø���Ч���ί����ٰ��D(zhu��n)�ơ�

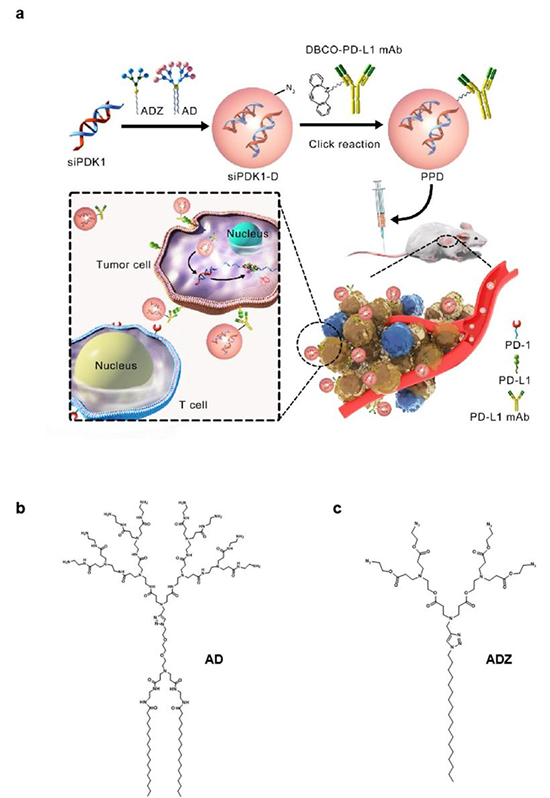
�D1 siPDK1-PD-L1���w���η��ӏ�(f��)���w��PPD���Ę�(g��u)��ʾ��D��a) PPD�Ę�(g��u)���Ͱ����ĬPDK1�Ŀ������Ե�ʾ��D��b) ����siRNA�f�͵Ď��а���ĩ�˵ă��H�Ԙ��η���AD�Ļ��W(xu��)�Y(ji��)��(g��u)��c�������c������(y��ng)�Ď��ЯB��ĩ�˵ă��H�Ԙ��η���ADZ�Ļ��W(xu��)�Y(ji��)��(g��u)��
����朽ӣ�https://onlinelibrary.wiley.com/doi/10.1002/adma.202305215
- ���_��W(xu��)ꐴ�ȫ����/�L����(y��ng)�������A���о��T��CD47KO/CRT�p���﹤�̼�(x��)��Ĥ�����{������(li��n)�Ͽ�PD-L1���w�����[�������ί� 2022-10-14
- ��������˹-�Rِ��W(xu��)����/�Ї�ˎ�t�/�۴��S˼�R ACS AMI�����H�Ԙ��η��Ӱ��������R����ᘌ��D(zhu��n)�����ѳ�������Ч�ί����� 2025-01-06
- ����CNRS����F(tu��n)� PNAS���{��ˎ���f��ϵ�y(t��ng) - �ԽM�b���η��ӳ����Ӽ{���z��ͨ�^�ٳּ�(x��)�������ݵķ�ʽ����f�Ϳ���ˎ�� 2023-06-07
- CNRS�����о��T���Ї�ˎ�t诽��� PNAS������bola�̓��H�Ԙ��η��ӌ��F(xi��n)����ˎ���x���Ժ��m��(y��ng)���f�� 2023-06-05
- ����W(xu��)�Ζ|�½����n�}�M Angew��������ƿˢ�ԽM�b��(g��u)���{����߶ȹ�W(xu��)�Y(ji��)��(g��u) 2025-05-15
- �|���֘I(y��)��W(xu��)�����½��ڈF(tu��n)� Small���Ҵ��錧(d��o)���z���ԽM�b���F(xi��n)���Іξ��ΑB(t��i)�Ϳ��{(di��o)�Y(ji��)��(g��u)��������̿ 2025-05-02
- ��(f��)����W(xu��)�������F(tu��n)� Macromolecules��ͻ���ԽM�b���g(sh��)��߅�� - �߹̺�����Ƕ�ι�����ğ��T��(d��o)�ԽM�b�c���T��(d��o)�f(xi��)ͬ�ԽM�b 2025-04-27
�\���P(gu��n)ע�߷��ӿƼ�

- �������C����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �������S���e���ڈF(tu��n)� Angew...
- ���ϴ�W(xu��)����/�S�M(j��n)�F(tu��n)� AFM:...
- ���T��W(xu��)�������n�}�M Sci. ...
- �A���r(n��ng)�������/����...
- ��h�������l(w��i)�ֽ��ڡ���P��...
- ��ʿ�m��W(xu��)�������F(tu��n)� Adv. ...
- ��h��W(xu��)�������ڈF(tu��n)ꠡ�Adv....
- ��������Rͬ�c���ڈF(tu��n)ꠡ�Sc...
- �Ϲ����غ������đ�Ƽ/�п�...
- ���T��W(xu��)�ܱ���F(tu��n)� ACS Nan...
- �V����W(xu��)���P���ڈF(tu��n)� CEJ...