�ϳɸ��dˎ���ļ{��ˎ��һֱ��һ험O��������΄գ������F��{��ˎ����ձ��m�á��B�m������Ҏģ���a�����y�ϼ��y���������Ĵ���W����|���ڡ�ꐾ��ɽ����c��۳��д�W�T�������ڈF������������һ�N���ڶ��-������s����ĿɔUչ���ώ죬�ɹ����F�˳����dˎ���{��ˎ��ĸ�Ч�B�m���a��ԓ�о��ɹ��l����Advanced Materials�ڿ��ϡ�
����c��
��ܲ��ώ죺���о�ͨ�^�x��ͬ�İ����ᣬ�ṩ��һ�N���-������s�����z�w����ώ졣ԓ�����܉_�{���d�w���P�I���ԣ����dˎ������������ԡ��R��ۼ���ȵȣ��鲻ͬ���È����ṩ�˶��ӻ����x��
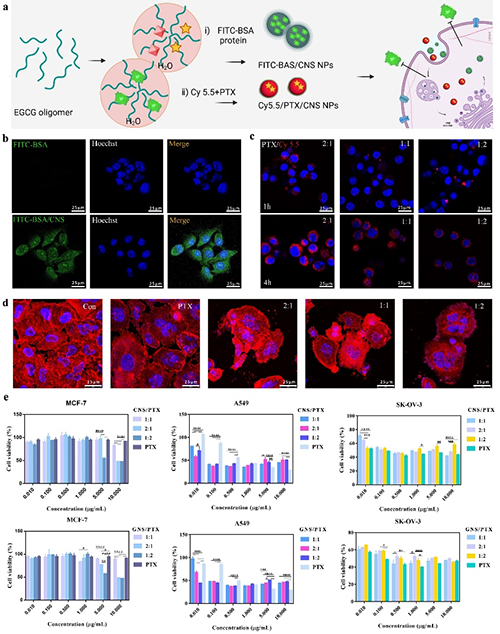
�����dˎ����ͨ�^�܄��錧�Ŀs����ֽ��c�ؽM����ɼ����PTX�����dˎ����� 86%�����ڶ�N�y����ˎ����ӣ��dˎ�������^50%���@ʾ���V�����m���ԡ�
�B�m�����a���������ؼ��g���{��ˎ������aЧ�ʿ��_5 mL/min��ÿ��36�ˣ����Ҽ{���w���ijߴ�ɾ��_�{�أ����ɢָ����PDI������0.2��
�������
Ŀǰ���s40%���Ј���ˎ���90%���R�����xˎ�����ˮ���Բ�Ć��}���������������öȵ͡���Ч���ޡ����y�ļ{��ˎ���f��ϵ�yͨ���dˎ���^�ͣ�<10%������Ҫ��νoˎ�ʹ����d�w���������ί����s�Ժ͝��ڵĽ����L�U����ˣ��_�l���dˎ���ļ{��ˎ���f��ϵ�y����ü�ޡ���ˎ��ͨ�^��ĥ����̎���߉����|���ȷ����������{�׳߶ȣ������a��ˎ�ﺬ���{���w������{��ˎ�����ֱ�ӷ���֮һ��Ȼ�����@�N����ͨ����Ҫ��������߉�ݔ�룬�ҳߴ�s�p��Ч���ܵ����ƣ��e�nj���100�{�����µļ{���w�������⣬ԓ�^��ͨ����Ҫʹ�Ì��T�ķ���������Һ���ͼ{�׳������ǏV�������Ƃ��dˎ�ۺ���{���w���ļ��g��ʹ�þۺ��ﱡĤˮ�����Ƃ��(2-�f����)�ۺ���{���w���r�����d��ɼ����PTX���ͽ��S�ص��dˎ�����_56%���c��Һ����ȣ��{�׳������ṩ�˸����Ρ����߳ɱ�Ч��ķ��������ҟo���ⲿ����ݔ�롣ͨ�^�C���W����ͨ�����ďV���Y�x���ѽ��b�����N���и��dˎ�����ԽM�b�{���w�������⣬���ö����Y��-�{���w���M�b�A�y��QSNAP��ģ���_�l��һ�N����Ⱦ�ϵİ����f��ϵ�y��ԓϵ�y���F�˘O�ߵ��dˎˮƽ��һ�N��ȿ��Ƶ��B�m�{�׳��������Q���}�T���{�׳��������ѱ��_�l���������dˎ�����_66.5 wt%�ľۺ���{���w������ģ�巨Ҳ����������Ƃ�o�d�w�{��ˎ������@Щ�������B�m���a�ܵ���Nԭ������ơ�
���ؼ{�׳������gͨ�^�������w�Uɢ����ϡ��黯����M�ϣ����F�˸��N�{�ײ��ϵ��B�m���a�����ؼ��g�����@���ă��ݣ������Ԅӻ���������aЧ�ʺͿ��؏��ԡ�����ϵ�y�Ќ����w��τ����W�ͭh�������ľ��_���ƃ������ԽM�b�^�̣����M�˿������a�������O��ķ��]���|Ҳ֧�֟o���w���Ƃ䡣�M�����ؼ��g�ё����ںϳɸ��N�dˎ�{���w�����������d�wͨ�����F�����dˎ�������磬ʹ�����Ӿ۽������O��r��mPEG-PLGA�����S�ص�����dˎЧ�ʞ�3.4%����ʹ�����ؼ��g�M�b����ɼ���dˎPLGA�{���w���У��dˎ�������s��1%��7%�����ؼ��g�����a�{��ˎ�����Ҫ���d���g���������a���dˎ���{��ˎ���I�����r��̽����
���·�����
����|���ڈF�һֱ������ͨ�^��Ȼ��������_�l�ί��Լ{���ܲ��ϣ������������ż�Ķ����J. Am. Chem. Soc. 2013, 135, 4179?4182�����������_�ɿصĵ���Ӽ{������J. Mater. Chem. B, 2018,6, 1373�����ۺ϶�Ӷ�ܲ��ϣ�ACS Appl. Mater. Interfaces 2020, 12, 34, 37914-37928��ACS Appl. Mater. Interfaces 2020, 12, 30, 33550-33563��ACS Sustainable Chemistry & Engineering��J. Mater. Chem. B 2023, 11, 11505-11518������ʳ�ó�С��Ӽ{��ø��Chemical Engineering Journal 500 (2024) 157090����
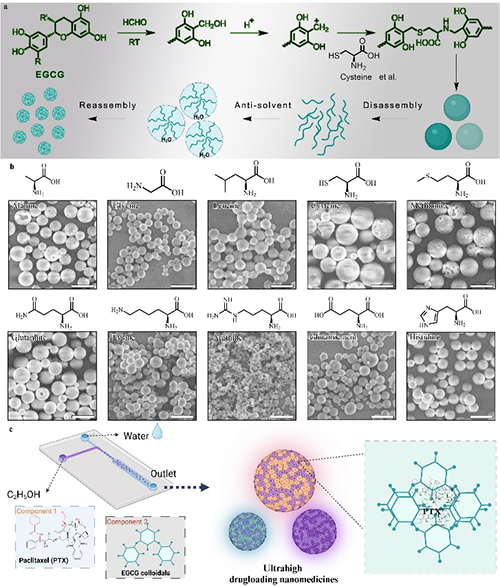
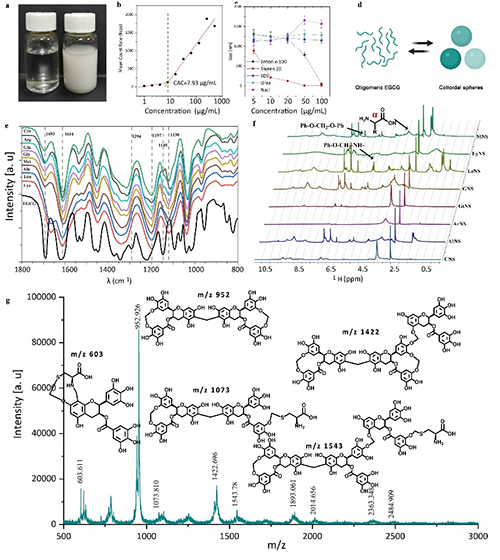
���о����F�����Ȼ���ӣ�EGCG����ԭ�ϣ�ͨ�^�x��ͬ�İ����ᣬ������һ�����-�������z�w��죬�@Щ�z�w��߂���؏ͽ�M�b���ٽM�b�����ܡ��о��ˆT���������ؼ��g�z�w������ܽY�ϣ�ͬ�r���F�˸��dˎ�����B�m��ͨ�����a��ԓ�о����H��{��ˎ��ĸ�Ч���a�ṩ����˼·��߀���Q�y����ˎ����f���y�}�ṩ�˄��·��������ڶ�ӵļ{���d�w���H���и��dˎ����߀�߂䃞�������������Ժ��ί�Ч����δ���������[���ί����װY�Լ����ί����I��l�]��Ҫ���á�





Փ����Ϣ��
A Library of Polyphenol-Amino Acid Condensates for High-Throughput Continuous Flow Production of Nanomedicines with Ultra-High Drug Loading
Zeng Yi, Xiaomin Ma, Qiulan Tong, Lei Ma, Yunfei Tan, Danni Liu, Chaoliang Tan*, Junze Chen*, Xudong Li*������|���Ĵ���W��
Advanced Materials, 2025, DOI: 10.1002/adma.202417534
https://doi.org/10.1002/adma.202417534
��һ������Ϣ��B
�������Ĵ���W�����t�W���̌WԺ�����Ѝ����о��T����Ҫ��������Ȼ����ܲ��Ϻͼ{��ˎ���� �ڽM���ޏ͡�����ϵ�y�������[���������P�о�����Advanced Materials, Chemical Engineering Journal��Green Chemistry, ACS Appl. Mater. Interfaces, ACS Sustainable Chemistry & Engineering, Carbohyd. Polym., J. Mater. Chem. B, ACS Biomaterials Science & Engineering, Colloids and Surfaces B Biointerfaces, ACS Applied Nano Materials���ڿ��l��ϵ��SCIՓ�ģ��о��ɹ����xACS Editors�� Choice�����]���c���£�J. Mater. Chem. B HOT paper��Ŀ���@�ڙ����Ұl������4헡�
�R�������Ĵ���W�A���tԺ�����Ѝ����о��T���@��������Ȼ�ƌW���������Ŀ���Ĵ�ʡ��Ȼ�ƌW���������Ŀ�ȶ�헻����֧�֡���Ҫ�����������f��ƽ�_�Ę��������ں���ϵ�y���P���������\���еđ����о�������Adv. Mater.��Adv. Healthc. Mater.��Chem. Eng. J.��Carbohyd. Polym.��ACS Appl. Mater. Interfaces��Inorg. Chem.��J. Mater. Chem. B��ACS Sustainable Chem. Eng.��Colloid. Surface. B��ACS Appl. Nano Mater.���ڿ��l����ƪSCIՓ�ġ�
ͨӍ������Ϣ��B
�T��������۳��д�W늙C����ϵ�K�������ڣ����������҃���������𣨸۰ģ��@���ߣ�2021����2024�ꮔ�x�����H���M���υf����ʿ����2018-2024���B�m7�����x��ȫ��߱����ƌW���������Ψ������2020-2024���B�m5�����x������ǰ2%�ƌW������˹̹����W����2022-2024���B�m3�����x��ȫ��피�ǰ10�f�ƌW������Σ�ȫ��W�ߎ죩���о��漰���S���ϡ�������������̽�y�����˹�����оƬ������{�ײ��Ϻͼ{���t�W�ȶ��W�ƽ����I����Nature��Nat. Nanotechnol.��Nat. Rev. Mater.��Chem. Rev.��Chem. Soc. Rev.��Nat. Commun.��Adv. Mater.��J. Am. Chem. Soc.��Angew. Chem. Int. Ed.�ȇ��H֪���ڿ��ϰl��SCIՓ��190��ƪ������39ƪ���xESI�߱���Փ�ģ�Փ�Ŀ�����33000��Σ�H����83�����Ρ�Smart Materials and Devices�������������Ρ��������W�W����Science Bulletin������Nanomaterials���͡�Energies����ί��2023��Advanced Materials�ڿ�������֮������2022��Small�ڿ�������֮������2023��Materials Chemistry Frontiers�ڿ���2021��Journal of Materials Chemistry A�ڿ������J�ƌW������
ꐾ������Ĵ���W��Ƹ�о��T���������Ĵ���W�p���˲��Ŀ���x�ߡ���Ҫ���¼{���|�Y����Һ���Ƃ��c�����о�������Nat. Chem.��Nat. Commun.��J. Am. Chem. Soc.��Angew. Chem. Int. Ed.��Adv. Mater.��Chem. Rev. �ȇ��H����SCI�W�g�ڿ��ϰl��Փ��40��ƪ������8000��Ρ��ڙ�����3헡�
����|���Ĵ���W�������ڣ�����������Ȼ���ӹ��ܼ{������ȡ����һϵ���о��ɹ���������Ȼ�������T���IJ����ԽM�b��ģ�K���`���{�ز��Ӽ{�������ܡ����Ӆfͬ����ί�������Ȼ��ӷ����鄩������-���S�����ί�AKI�Ͳ���Pickering�鄩ϵ�й������@Щ��������Ȼ���ӹ��ܷ����D������й������õ��d�wƽ�_������Ȼ������ͼ{�ײ��ϵĺ����OӋ���Ƃ��ṩ���µ�ƽ�_���g�����O�����M��Ȼ����²��ϵ��_�l���á��L�ڏ��½M���ޏ��c�����ü{�Y��/����������Ϻ�ֲ�����YԴ���õ��о����Ⱥ�Г�����973Ӌ���Ŀ�n�}��������Ȼ�ƌW����ί�Ŀ���Ĵ�ʡ�Ƽ����P�Ŀ���l��һϵ�е��о�Փ�ĺͫ@ʮ�����ڙ����Ұl��������Փ�ijɹ����xӢ���ʼһ��W�����������W������Ȼ�Ї��о����c���]��
- �пƴ�������/�Y��F� Nat. Biomed. Eng.: ����һ��������NO��ͻ���[��Ѫ�ܻ���Ĥ���ϣ������{��ˎ�������f�� 2025-05-03
- �칤����x/��ԕ��F� Acta Biomater.�������p�Ҷ�ܼ{��ˎ��˷��ߺ���U���錧�ĽYֱ�c��������ˎ�c�������� 2025-02-11
- �Ϸ��t����������� Biomaterials: �пս�����������F�{��ˎ��錧������Fe3+/2+ѭ�h�����ڴ��[���F�����ί� 2024-11-01
- Science��AI��ͨ���Y�ϵ���������OӋ���ٲ��ϰl�F 2024-12-14
- ��������·���ڈF�2023����гɹ����\ 2024-02-11
- �Ͽϴ�W�Ρ���ڈF� Adv. Funct. Mater.: Һ���ؽM���]�{���w�S��������ͨ���{�VĤ 2024-01-07
