���գ������������W(xu��)Ժ�߂������n�}�M�c�ϼ��ݴ�W(xu��)�����ݴ�W(xu��)��ɼ����У�ȶ���피���ЙC��(g��u)��������Science���ϰl(f��)����������Imaging-guided deep tissue in vivo sound printing�����о������¡�����������ʿ��Elham Davoodi���һ���ߡ�
�@헹���������һ���O��ͻ���Ե��·������������(q��)�ӵĻ��w�����(zh��n)3D��ӡ���g(sh��)�����Q DISP��Deep tissue in vivo sound printing�����о��F(tu��n)��_�l(f��)��һ�N�Ծ۽�����FUS�����(q��)��Դ���Y(ji��)�Ϝ���֬�|(zh��)�w��LTSLs���͚������ݣ�GVs������Ķ��ƽ�_��ʹ�ƌW(xu��)�҂��״��܉�������(d��ng)�����P����ֱ���ڻ��w��̎����(zh��n)������������ӡ����(d��o)늡�ˎ��ؓ(f��)�d����(x��)������ͽM��ճ���ȶ��ӻ����ܵ�ˮ���z�Y(ji��)��(g��u)���@헼��g(sh��)���H��С������[��ģ�͡������Ȳ�����ȏ�(f��)�s�����h(hu��n)��������˳ɹ���C��߀���w��(n��i)չ�F(xi��n)����(y��u)�������������ԣ�����(chu��ng)�t(y��)�������Ի��ί��������t(y��)�W(xu��)�ȷ����_������·����
DISP ƽ�_�ļ��g(sh��)������һ���߶�����ĽM�ϡ��о��ˆT�O(sh��)Ӌ�������������ī��US-ink�����ɽ�(li��n)�����b�ڵ͜���֬�|(zh��)�w�У������·�(w��n)�����ڣ������c�܇��M������ϰl(f��)����ǰ����(y��ng)������(d��ng)�۽���������(zh��n)Ŀ��(bi��o)�^(q��)��ֲ��ضȕ������_�������s41�C43�z�϶ȣ��T�l(f��)֬�|(zh��)�w����׃��ጷų���(li��n)����ʹ��ī��ָ��λ��Ѹ��������z�����@�N�����|�l(f��)���ֲ�����(zh��n)�Ľ�(li��n)��ʽ���H�����˂��y(t��ng)�A(y��)�����ī���ڵĶ��Ժͷ���(y��ng)��(w��n)���Ԇ��}��߀�ܼ����x���͡����ɻ��͡������͵ȶ�N��(li��n)�C�ơ�����Ҫ���ǣ�DISP ϵ�y(t��ng)�����˚����������鳬����Č��Ȅ���ʹ�о��ˆT���ڌ��r��������(d��o)�¾���(zh��n)��λ��ī���O(ji��n)�y��ӡ�M(j��n)�̡��_�J(r��n)��(li��n)Ч�����������˲����Ŀɿ����c�ɿ��ԡ�
�@헼��g(sh��)�����ܴ�ӡ��ʲô���о��F(tu��n)�չʾ�������@�@�Ķ��ӻ��ɹ������Ì�(d��o)�ˮ���z�������ɹ����w��(n��i)��ӡ���Y(ji��)��̼�{�ܡ��y�{�������ӄ����·�Y(ji��)��(g��u)�����H�߂����õ����̖����(d��o)������߀�������졢���۵șCе׃���±���(d��o)늷�(w��n)���ԣ�����늈D��ECG������늈D��EMG�����w�رO(ji��n)�y��ֲ��ʽ�������ṩ��ȫ�·�������ͨ�^��ˮ���z��Ƕ��С����ˎ������|(zh��)����ᣬDISP ��ֱ�����[������^(q��)���ӡˎ��죬���F(xi��n)����(zh��n)��λ�����m(x��)ጷš��p��ȫ�������á����⣬����߀���w��(n��i)�ɹ���ӡ�˰���(x��)����ˮ���z������ģ�M�M���������ޏ�(f��)�������@ʾ������M�����̡��ɼ�(x��)�������ṩ֧�ֵĝ������������ڴ����ǣ��F(tu��n)��_�l(f��)�˾��Џ���ճ������������ˮ���z���܉����ܓp�M������ֱ�Ӵ�ӡ�γɸߏ��ȵķ��]���棬��(y��ng)����ֹѪ�����ڷ��]�����ٽӿ��ܷ�ȣ�δ�����S�ܞ����g(sh��)���Ⱥ���(chu��ng)�ޏ�(f��)�ṩ�µĹ��ߡ�
�ڄ����У��о��ˆT�� DISP ���g(sh��)��(y��ng)����С������[��ģ�ͺ������Ȳ����⣬�����C��������Ժ;��_�ԡ������^���У�������īͨ�^ע���?q��)���ݔ�͵��w��(n��i)ָ����λ�����۽����ڌ��r��������(d��o)�¾��_���衢�ֲ����l(f��)��(li��n)��ጷţ��ڲ����l(f��)�܇��M���p���ėl���£���ɏ�(f��)�s�Π�Y(ji��)��(g��u)�Ĵ�ӡ���M���W(xu��)��������HEȾɫ�����ߟɹ��(bi��o)ӛ���������oՓ����ī����߀�Ǵ�ӡ���ͺ��ˮ���z�������F(xi��n)����(y��u)�������������ԣ������l(f��)���@�װY�����߽�����M���������������w��(n��i)�Ľ��⡢��(w��n)���Ա��F(xi��n)Ҳ�����t(y��)�������eֵ��һ����ǣ�ԓ�о�߀չʾ�˽Y(ji��)�� GV Ca2? ���������·f�������������w��(n��i)���rۙ��(li��n)�^���c���Ͽ��g�ֲ�������˲����Ŀ�Ҋ�ԺͰ�ȫ�ԡ�
չ��δ����DISP ���g(sh��)�Н������ܶ�N�t(y��)����(y��ng)�È����������[������(zh��n)�ί���������ֱ�Ӱ�ˎ����ϴ�ӡ�������܇����p��ȫ����ˎ�ﱩ¶�����ڽM���ޏ�(f��)�c�����������������a����һ�����ܓp�^(q��)��ֱ�Ә�(g��u)���ޏ�(f��)֧�ܻ�(x��)���d�w�������w��(n��i)�ɴ�����ӌW(xu��)�������܌��F(xi��n)�o��(chu��ng)ֲ�����������(d��o)����늘O��������һ���w��(n��i)-�w�⽻��ϵ�y(t��ng)���@���H��3D��ӡ���g(sh��)��ͻ�ƣ����Ǿ���(zh��n)�t(y��)�������������Ի����o��(chu��ng)������Ҫһ������(d��ng)Ȼ��DISP Ҳ���R�T������(zh��n)����������m��(y��ng)��(f��)�s�ӑB(t��i)���٣������K���β������\�ӡ����(y��u)��������(sh��)�cϵ�y(t��ng)푑�(y��ng)����ο�Խ�Ą�����w�R���ľ��D(zhu��n)���T���ȣ��@Щ����Ҫ��W(xu��)�Ƶ�����̽���c�f(xi��)����
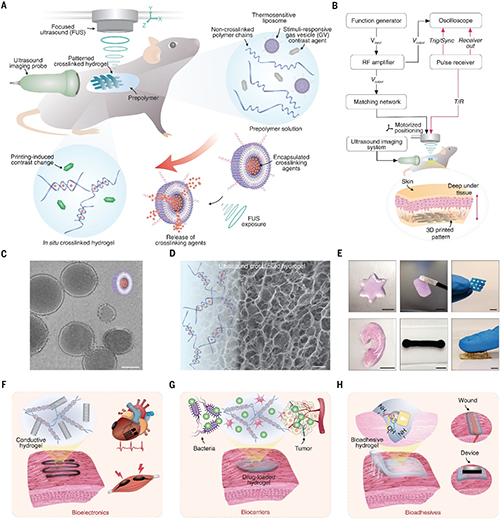
�D1. ���ڳ�������(d��o)�Ļ��w�����ӡ��DISP��ʾ��D��ͨ�^�۽�����FUS���(q��)�Ӻ͚������ݣ�GVs�����r���Y(ji��)�Ϝ���֬�|(zh��)�w��LTSLs�����b�Ľ�(li��n)�������F(xi��n)�ڻ��w�M�������ጷŲ���(li��n)������ī����(g��u)����(d��o)늡�ˎ��ؓ(f��)�d����(x��)������ȶ��ˮ���z�Y(ji��)��(g��u)���龫��(zh��n)�ί��������t(y��)�W(xu��)�ṩ�o��(chu��ng)������(zh��n)�����w���췽����
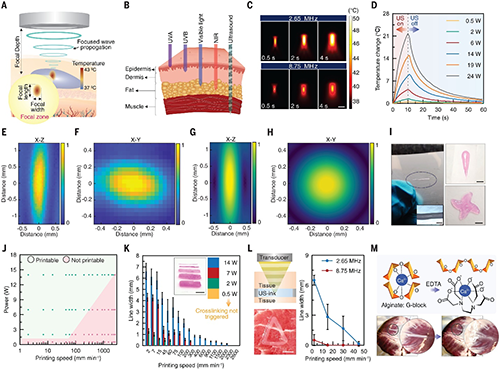
�D2. �о�չʾ�˾۽�����FUS���(q��)�ӵ����S��ӡ���ԡ������ܾ���(zh��n)���M������������ī��(zh��n)�_��λ������Ȃ��y(t��ng)������⡢���t��ȹ�Դ���и����Ĵ�������ģ�M�Y(ji��)���@ʾ���ڲ�ͬ�l�ʺ�����r�g�£��۽��^(q��)��Ĝضȷֲ��߶ȿɿأ��������ֲ�����cģ�MҲ�C���˳��۽��ľ���(zh��n)�ԡ��о��F(tu��n)������@һϵ�y(t��ng)��ӡ������(x��)��ˮ���z�D�����ڲ�ͬ���ʺʹ�ӡ�ٶ��£��������}��ī���F(xi��n)�����õĴ�ӡ�ֱ��ʣ������ܴ� 15 ������i��M��������ӡ�����⣬�@Щ��ӡ����ˮ���z�D��߀��ͨ�^���εĻ��W(xu��)̎�����ٽ��x�����w��(n��i)������������ṩ����;����
���w���ԣ��@헁��Լ��������W(xu��)Ժ���ϼ��ݴ�W(xu��)��UCLA ��피���ЈF(tu��n)꠵Ĺ�����չʾ�����������P�����ڻ��w��(n��i)����(zh��n)����������ϵľ�����δ�����S���@헼��g(sh��)�IJ�����(y��u)������չ�������S���ɞ���(chu��ng)�t(y��)���������t(y��)�W(xu��)���w��(n��i)��ӌW(xu��)���I(l��ng)��ĺ��Ĺ��ߣ��Ƅ������t(y��)�W(xu��)�M(j��n)��һ��ȫ�µķ�ʽ�r�������������ȫ������Ч��������(zh��n)�t(y��)�����������������f���@�o����һ�������Ե��M(j��n)����
ԭ��朽ӣ�https://www.science.org/doi/10.1126/science.adt0293
- ������������ֽ��ڡ����½��ڡ��w�θ����ڈF(tu��n)� NSR������ˎ��(x��)����Ⱦ���\�Ӳ�λ��(chu��ng)��ȫ�^�̹�����ȡ�����M(j��n)չ 2025-06-12
- ɽ�|��W(xu��) Nat. Mater.����푑�(y��ng)��늼{���NƬ�{(di��o)����(j��ng)�ɼ�(x��)���ֻ��ί���(chu��ng)�����X�p�� 2025-05-09
- ��������W(xu��)����n�}�M Adv. Sci.: ���ó��ջ��Ŀ��١��o���l(f��)���ĸ�����ˮ���z�Ƃ䷽�� 2025-04-24
- �����ģ����ڣ��Ʊ���Ժʿ�����ڴ�W(xu��)���|���ڵ� Nat. Protoc.: NIR-II���l(f��)AIE�����{�����ڷνY(ji��)�˻��w��W(xu��)�\�� 2025-04-18
- ��ɽ��W(xu��)�Z�Ѿ��n�}�M AHM: ���b�ס����w������ƽ�_ - ����Ⱦ�������ϵĄ�(chu��ng)�½�Q���� 2025-01-25
- �Ϻ����M��F(tu��n)� Adv. Sci.����(x��)�����w̽ᘵ��Ƃ估�����c�\����(y��ng)�� 2023-12-05
- �A���삥/�����ֿƴ����H� AM���p�ظ������������i��������(x��)�����S����������ľ�R�� ֮��-����(zh��n)�{(di��o)��(ji��)�c����Ⱥ�������˝����ԽY(ji��)�c�� 2025-06-09
�\���P(gu��n)ע�߷��ӿƼ�

- �������C����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �������S���e���ڈF(tu��n)� Angew...
- ���ϴ�W(xu��)����/�S�M(j��n)�F(tu��n)� AFM:...
- ���T��W(xu��)�������n�}�M Sci. ...
- �A���r(n��ng)�������/����...
- ��h�������l(w��i)�ֽ��ڡ���P��...
- ��ʿ�m��W(xu��)�������F(tu��n)� Adv. ...
- ��h��W(xu��)�������ڈF(tu��n)ꠡ�Adv....
- ��������Rͬ�c���ڈF(tu��n)ꠡ�Sc...
- �Ϲ����غ������đ�Ƽ/�п�...
- ���T��W(xu��)�ܱ���F(tu��n)� ACS Nan...
- �V����W(xu��)���P���ڈF(tu��n)� CEJ...