����ί������ù���D�Q�{���w���ڽ��t�⼤�������£����[����λ�a���ֲ��ߜ횢���[�����������и߶��x���ԡ�Ȼ����Ŀǰ���ڼ{���w���Ĺ���ί��c�R���[���ί��Դ���һЩ��࣬�@�����ڼ{���w����β�o�}ע��oˎ��ֻ�зdz������ļ{���w����ݔ�͵��[����λ���@ʹ�������y�����w�Ȱl�]�߯�Ч���Ķ����������R�����á���Ό��F�{���w��������ϵ�y���ݺ��Lѭ�h�Ǵ��M�{���w�����[����λ�����ͫ@���������ί�Ч�����P�I��
����Ĥ���܉��x��{���w��Դ�����������еĹ��ܺ����|���Ҳ�ͬ��ͼ������s��Ĥ����Ϳ�����{���w�����棬�x��{���w����ܡ��ܴˆ��l���͵���W�߷��ӿƌWϵ�����������n�}�M��ǰ�ڹ��� (Biomaterials, 2017, 143, 29)�Ļ��A�ϣ����t����(RBC)Ĥ�c���ٰ�����(MCF-7)Ĥ�ںϣ��Ƃ��˼t����-�������s��Ĥ���µĺ�ɫ�ؼ{������(Melanin@RBC-M)���Mһ�������[���Ĺ���ί�(��D1��ʾ)��
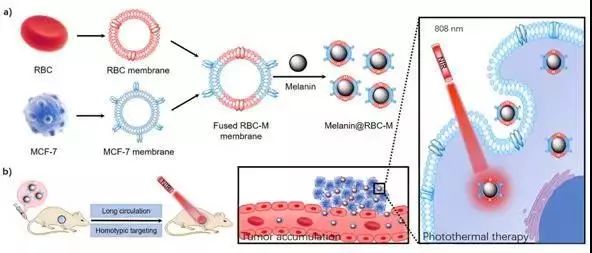
�D1 �t����-������Ĥ���µĺ�ɫ�ؼ{������(Melanin@RBC-M)���������[���Ĺ���ί���
�о��l�F���ںϵ�RBC-M�s��Ĥ����ͬ�r����RBC��MCF-7����Ĥ���ף����Ƃ��Melanin@RBC-M�ͺϼ{������ͬ�r�������L��ѪҺѭ�h�r�g�Ͱ�����ͬԴ�����ԡ����s��Ĥ(RBC-M)������MCF-7Ĥ�M�ֿ��@������Melanin@RBC-M�{�����ӵ�ͬԴ�����ܣ����s��Ĥ��RBCĤ�M�ֵ����ӿ���Ч�p�پ��ɼ����zȡMelanin@RBC-M�ͺϼ{�����ӣ����L��ѪҺѭ�h�r�g (��D2��ʾ)��
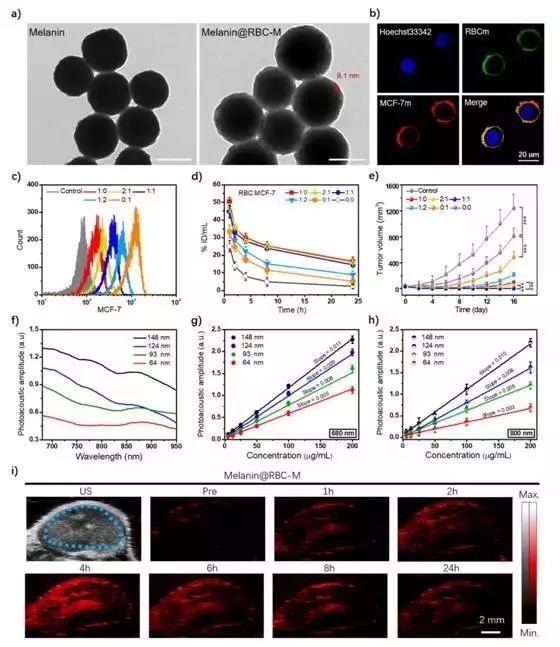
�D2 a) ����ɫ�ؼ{�����Ӻͼt����-�������s��Ĥ���µĺ�ɫ�ؼ{�����ӵ����u��ؓȾ�������R�D, �˳ߞ�100 nm. b) �����ٰ������ͼt����-�������s��Ĥ���µĺ�ɫ�ؼ{�����ӹ�������Ĺ��۽�����D, �˳ߞ�20 ��m. c) ��ͬRBC�cMCF-7Ĥ���ױ��ص�Melanin@RBC-M�{�����������ٰ������е���ʽֱ���D. d) �t����-�������s��Ĥ���µĺ�ɫ�ؼ{�����Ӻͼ���ɫ�ؼ{�����ӵ�ˎ�������W����. e) �t����-�������s��Ĥ���µĺ�ɫ�ؼ{�����Ӻͼ���ɫ�ؼ{�����ӌ�MCF-7�[�����������L. f) ��ͬ�ߴ�Melanin@RBC-M �{�����ӵĹ���̖�D�V. g-h) ��ͬ�ߴ�Melanin@RBC-M�{�����ӷքe��680 nm (g) ��800 nm (h) ���l���L�µĹ����ֵ�S�{�����ӝ��׃���������D. i) �t����-�������s��Ĥ���µĺ�ɫ�ؼ{������(i.e. 124 nm)���[����λ�ij���������.
������������ڌ��F���Lѭ�h��ͬԴ����֮�g��ƽ�⣬RBC�cMCF-7Ĥ���������Ȟ�1:1�Ļ��Ĥ���Melanin@RBC-M�ͺϼ{�����ӣ����^������Ĥ���������ȵ�Melanin@RBC-M�����ĺ�ɫ�ؼ{�����ӣ����F���@���������[����λ��������ί�Ч��������808 nm���t�����10��犣����^�͵Ĺ���ܶ���(1 W/cm2)������ȫ�����[�������⣬�w�������Y���������S����ɫ�غ����ӳߴ������(64 �� 148 nm)��Melanin@RBC-M�ͺϼ{�����Ӿ��������Ĺ���̖������680 �C 800 nm �����ļ��l���L�£������ֵ�S�{�����ӵĝ�Ⱦ������ӣ������ڶ����y��Melanin@RBC-M���w�ȵ�����ֲ����@�N�s��Ĥ���¼{���w���ķ����������{�����ӵĹ����ԺͿɿ��ԣ������ƄӼ{���g���õķ����ڂ��w�t����
���P�о��ɹ����ھ��l����Biomaterials�ϡ�Փ�ĵ�һ���ߞ�͵���W�߷��ӿƌWϵ��ʿ���������߷��ӿƌWϵ������������ˎ�WԺ��־�帱�о��T��ԓ���µĹ�ͬͨӍ���ߡ�
Ԕ��ՈҊ��
Erythrocyte-cancer hybrid membrane-camouflaged melanin nanoparticles forenhancing photothermal therapy efficacy in tumors, Biomaterials 2019, 192: 292-308.
- ���ϴ�W��ӡ���� Angew���ξ��w���Ȳ��^�Y���Ŀ��g�{�� 2025-05-05
- �|�A��W�����ΈF� Macromolecules��ܛ�{���������w��׃��ʾ���p�Y��ԭ���͘O�� 2025-04-17
- �㽭��W����Fꠡ�Adv. Sci.��������ʽ�{�������T�������~�������ڸ�Ⱦ�Է����ί� 2025-02-27
- �칤����x/�R�w�R/���ƽ� Small����ˮ�˺�/�͜ع��fͬ�����[���ί� 2025-07-11
- �K���־�h/�������K��һԺ����� Nat. Commun.���[��Ѫ���m���ԡ�ճ���ԺͿ������������ڿɳ��m�Ľ����}���W˨���ί� 2025-07-09
- ���ݴ�W�����ƽ��ڈFꠡ�Acta Biomater.����ˎ����;ۺ���{���z�������[���LЧ�ί����о��ɹ� 2025-07-08
- �|�A��Wʷ��ꖽ���/�������о��T�F� AFM: �p�Ӽ{���R�_���ڸ�Ч�[������ί����ί����װY���� 2025-03-17
