���������Ժ��D(zhu��n)ȾЧ�ʸߵ���x�ӻ����d�w�ڻ����ί��I(l��ng)���ЏV���đ�(y��ng)��ǰ����Ŀǰ����(b��o)���Ļ����d�w���龀�Ծۺ�����Ƃ�l��ͨ���^���(y��n)�����ϳ��^����߀���ܕ�(hu��)���벻�׳�ȥ�Ľ����x�ӣ��Ķ��ڑ�(y��ng)���^��������~��ļ�(x��)�����ԡ�
���˽�Q�������}������������W(xu��)���ϿƌW(xu��)�c���̌W(xu��)Ժ�츣�����ڈF(tu��n)�(du��)ͨ�^��һ偷�����(g��u)�������p���I��֧����x�Ӿۺ��֧���ۺ���߶�֧������?f��)�Y(ji��)��(g��u)����(d��)�صă�(n��i)����ǻ�������ڻ���İ������c��ͬ�r(sh��)���ۺ���������p���I�����ڲ��ְ���(x��)����߀ԭ�ԗl�����ѣ���(sh��)�F(xi��n)�ۺ������Ч���⡣�@���H�ܽ��ͼ�(x��)�����ԣ�߀�ܴ��M(j��n)Ŀ��(bi��o)�����ጷţ��Ķ�����D(zhu��n)ȾЧ�ʡ�ʹ�ô���x�Ӿۺ��������d�w�\(y��n)�d�ɱ��_(d��)���(d��ng)�������|(zh��)������ͨ�^���(d��ng)���ί��(y��n)�C��(du��)�[����(x��)���Ě�������K��(g��u)����һ�N�Ͷ���Ч�ɽ�������ͻ����d�w��ԓ���������l(f��)���ڡ��߷��ӌW(xu��)��(b��o)��2019���6�ڡ������t(y��)�ø߷��ӡ�����
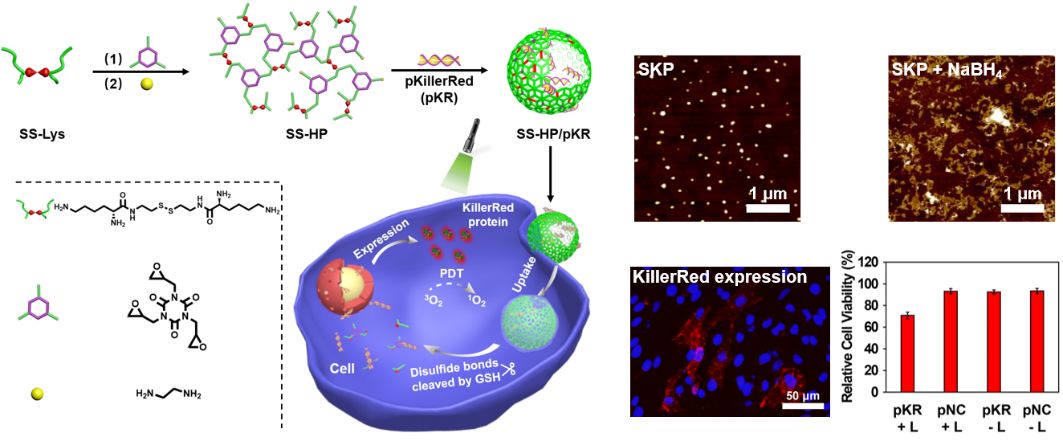
��������˼·��ԓՓ���x�����������Ժõ���ȻС����ه�������A(ch��)���c�װ�ͨ�^����������(y��ng)�õ������p���I�Ķష��������SS-Lys���S��ͨ�^SS-Lys�ϰ����c1,3,5-���sˮ����-s-�����ͪ(TGIC)�Эh(hu��n)�����F(tu��n)���_�h(hu��n)����(y��ng)��һ偷����õ�߀ԭ푑�(y��ng)�Ϳɽ���֧����x�Ӿۺ���SS-HP���@�N�_�h(hu��n)����(y��ng)�܉��ھۺ������γɴ������u�����Ķ�������x�Ӿۺ���IJ�����늺ɣ����;ۺ���ļ�(x��)�����ԣ��������L�ۺ����ѪҺѭ�h(hu��n)�r(sh��)�g��ԓ�ۺ����܉���Ч�؉��spDNA�γɾ�һ��(w��n)��������Լ{�����ӣ������w��ģ�M��߀ԭ�ԭh(hu��n)���п��Խ��⣬��(sh��)�F(xi��n)pDNAጷš�SS-HP��CC-HP���w���D(zhu��n)Ⱦ��������(x��)������ͨ�^�ɹ���ø��(b��o)������MTT�����X�z�|(zh��)��C6�ΰ�HepG2��(x��)���Мy������(sh��)�(y��n)�Y(ji��)��������SS-HP����Чؓ(f��)�dpDNA����(sh��)�F(xi��n)�ڰ���(x��)������Ч�D(zhu��n)Ⱦ����?y��n)�SS-HP�����ڼ�(x��)����(n��i)�����Լ����_�h(hu��n)����(y��ng)�o�d�w����Ĵ����u����ʹ�d�w���^�͵ļ�(x��)�����ԡ�KillerRed������һ�N�ڿ�Ҋ���������ܮa(ch��n)���ξ��B(t��i)���ļtɫ�ɹ⵰�ס�ʹ��SS-HP�y�dpKillerRed (pKR)�|(zh��)���M(j��n)���w����(d��ng)�������u(p��ng)�r(ji��)��SS-HP/pKR�D(zhu��n)ȾC6��(x��)�����ܳɹ����_(d��)��KillerRed���ף����պ���Դ��M(j��n)�[����(x��)���ĵ������@�N������Ȼ�����ᘋ(g��u)����߀ԭ푑�(y��ng)�Խ����֧����x�ӻ����d�w�����ͻ����d�w�İl(f��)չ�ṩ����˼·��
Փ��朽ӣ�http://www.gfzxb.org/fileGFZXB/journal/article/gfzxb/newcreate/gfzxb20180260xufujian.pdf
- ���������i�����n�}�M Sci. Adv.�����x���Ԛ���ESKAPE��ˎ���ĺ������H����x�Ӿۺ��� 2024-09-01
- �������Ʊ���Ժʿ/������α�� Angew������f-Ȳ�c(di��n)���ۺ� 2024-05-04
- �п�Ժ�������M(j��n)Ժ���L혈F(tu��n)�(du��) AFM��С������x�Ӿۺ�������(qi��ng)�������}����īˮ�Ĵ�ӡ�Ժ�������� 2023-12-14
- �|�A��W(xu��)�����/ʷ��ꖽ����n�}�M��ACS AMI������֦����Ӱ����~�K�p���ټ{��ø�����[���h(hu��n)���{(di��o)�ع��/������ 2025-06-19
- ���д����ڣ��w�� / �Ʊ��҈F(tu��n)�(du��) ACS Nano �����AIE�{���R�_(d��)ͻ���[������ - ��(sh��)�F(xi��n)����(zh��n)���\�� 2025-05-29
- ɽ�|��W(xu��)����ϼ���ڈF(tu��n)�(du��) Nat. Nanotech.���l(f��)�F(xi��n)��QCAR-T��(x��)��������(sh��)�w����Ч������Ч���� 2025-05-20
- ��ɽ��W(xu��)�����������n�}�M�����ξۺ�����������ˎ�ﹲ���f�d�w�о���ȡ�����M(j��n)չ 2021-02-01
�\���P(gu��n)ע�߷��ӿƼ�

- ����(b��o)���C(j��)��(hu��)��500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ�(hu��)�h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��(hu��)
- �Ј���300�|��PMEC China ɫ...
- ����ע��(c��)��2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �A�ƴ�Ǻ��� Sci. Adv.����...
- �칤��܊/���r�F(tu��n)�(du��) AFM...
- ���ϴ�W(xu��)Ƥ�������� Angew��...
- �Ĵ���W(xu��)�~�ֽ��ڈF(tu��n)�(du��) Small...
- ���A������W(xu��)�����n�}�M CEJ...
- ���ִ�W(xu��)�������n�}�M ACS M...
- �������S���e���ڈF(tu��n)�(du��) Angew...
- ���ϴ�W(xu��)����/�S�M(j��n)�F(tu��n)�(du��) AFM:...
- ���T��W(xu��)�������n�}�M Sci. ...
- �A���r(n��ng)�������/����...
- ��h�������l(w��i)�ֽ��ڡ���P��...