���ȍu���ۘӶ���(hIAPP)���e�`�ۯB�c�ۼ��Ɍ��ȍu�¼����a�����ԣ���2��������Ҫ�T����ˣ��lչ��Ч��ֹhIAPP�ۼ������Ƅ��܉������ί�2�����ĝ���ˎ����ˎ���cС���ӱ��^���и��Ժ����ﰲȫ�ԣ������܉��خ����R�e���ۘӵ��ף���˳ɞ��аlչ�����ĺ��xˎ�Ȼ�����������Ƅ�ͨ����ˮ�ԏ���ˮ���Ե��Լ��������^�����ĿǰһЩ������Ƅ��H�ڽӽ����WӋ�����������ߝ�ȕr����Ч����˼���lչһ�N�܉��Ч����������Ƅ�����Ч�ʵIJ��ԡ�

ǰ���_�����Ϸ���F��״Έ��˾��ж���������Ұ����������hIAPP����Ч���Ƅ�����������ͨ�^��-hIAPP �������ֹ hIAPP �ۼ���Ȼ���������^���Ұ����Ԫ������ 3���ĹѾ��Ұ������������ӵ���ˮ�Ժ͏��ҵ��Ծۼ��A��o�����Ƶ��ۘӵ������ɡ�ᘌ��������}���_���F��c���������@��о��к����lչ��һ�N�������Ѿ��Ұ���Ч���IJ��ԡ����������пɾ����ԡ������خ����Լ����a�Q���^ (CDR) �c��ԭ�ĸ��H�������{���w�ɞ������Ѿ��Ұ�������Ч������Ч���ԡ��ľ��Ұ��� YYYY (4Y) ���ӵ��{���w�ĵ������a�Q���^ (CDR3) �Ԙ����{���w N4Y���Ķ��̶�4Y�Ę����������c hIAPP �ĽY���H��������������4Y������Ч�������팢 N4Y �c�ۺ���N,N-�����Ҷ������Եľۣ���ϩ�ᣩ(PAA-DMA, or PD)ż���γɶ��r�ۺ���-�{���wż�� PAA-DMA-N4Y (PDN4Y), ��ͨ�^���rЧ�����F��4Y �Ķ��λ���D1����

�D1. �{���w N4Y �Ͷ��r����� PDN4Y ������IAPP�ۼ�����Ч�ʵIJ���
�о������÷��ӄ����Wģ�M�Լ�ELISA����C����4Y Ƭ���c hIAPP ֮�g�������ͨ�^N4Y�Ę��������Լ� PDN4Y �Ķ��rЧ���ּ��������D2-3����ThT�ɹ�����W��TEM���������Y�������ڷdz��͵Ļ��WӋ������£�4Y δ������ hIAPP �ۼ����� N4Y ��Ч�����t�� hIAPP �ۼ������֜p�p�� hIAPP ���ۘӵ������ɡ�Ȼ����PDN4Y �܉�ͨ�^�������ƺͶ��r�ąfͬ������ȫ���� hIAPP �ľۼ��͵��ۘӵ������ɣ��D4����

�D 2. (A) 4Y�Ę���(B) 4Y��hIAPP֮�g�ĽY�ϡ�(C) N4Yģ�ͣ������Ă�Y������CDR3��һ�Ȍ��R��(D)N4Y��hIAPP֮�g�ĽY��ģʽ������4Y�������tɫ������ͻ����ͨ�^��ˮ����ú� ��-�� ������chIAPP���Gɫ������á�
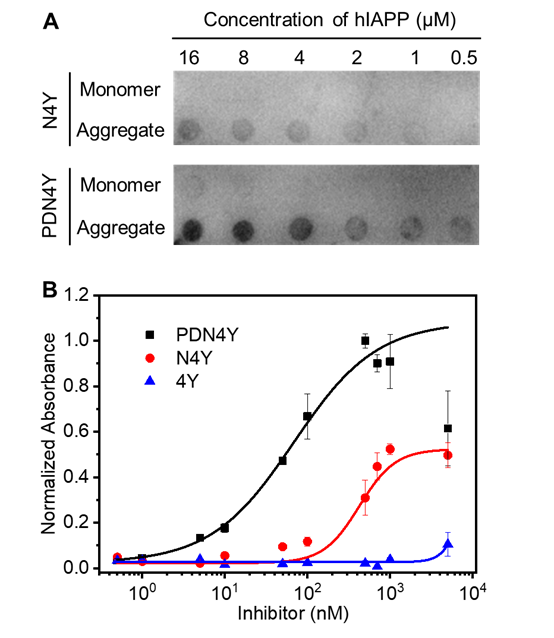
�D3. ����ӡ�E(A)��ELISA(B)����hIAPP �c��ͬ���Ƅ�֮�g�ĽY�ϻ��ԡ�

�D4. 4Y��N4Y��PDN4Y�ڲ�ͬĦ������hIAPP���ۘӵ������ɵ��������á�(A, B) ͨ�^ ThT�z�yhIAPP���ۘӵ���ԭ�w�S�M�b�Ą����W��hIAPP: ���Ƅ�Ħ���ȷքe�� 20:1 (A) �� 40:1 (B)��(C) hIAPP �����W����ڲ�ͬ���Ƅ������µĜ����ڕr�g��(D) hIAPP�ڄ����W���Y���r��TEM�D��
�о����ڼ���ˮƽ����C���@�N���Ԍ�hIAPP�Ѿ��w�T���ļ������Եķּ����⡣�Y���@ʾhIAPP�c�����ȍu�����������a��50%�ļ������ԣ�����4Y֮�������]������������N4Y��������������60%��������PDN4Y֮����������ȵ�80%���ϣ��D5����
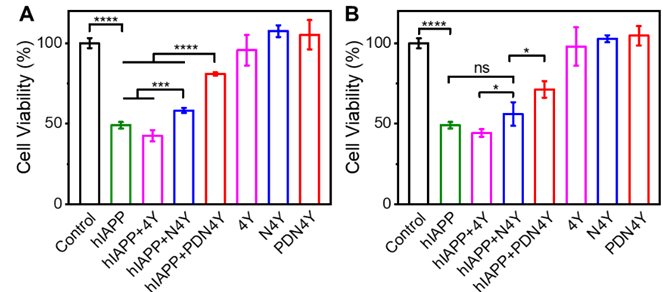
�D5. ��hIAPP:���Ƅ�Ħ���ȷքe��20:1 (A)��40:1 (B) ����r�£�ͨ�^ MTT �u���ڲ�ͬ���Ƅ���hIAPP�������Եķּ��������á�
�����ֹ��������P���������ȍu���ۘӵ����w�S�����о���Ҫ���ڼ���ˮƽ���w�⌍����M�еġ���������R�~�ѱ��������ۘ�׃���о����w��ģ�͡��о������ʹ�ð��R�~��̥���u����ͬ���Ƅ����w�Ȝp�p hIAPP ���ۘ�׃���T���Ķ��Է���Ĺ�Ч���Y���@ʾ���r�����PDN4Y�܉�ͨ�^�������ƺͶ��r�ąfͬ������Ч�p�p hIAPP �錧�Ķ��ԺͰ��R�~��̥�л����� (ROS) �Įa����

�D6. ���R�~��̥���Ժͻ����� (ROS) ���ɵ��w�șz�y��(A-B)���Ԝy��(A)��ROS���ɜy��(B)�İ��R�~����OӋʾ��D��(C) 72 hpf�r����������̥�Ĕ����� (D) DCF�z�yROS���ɡ� (E)������������̥�Ĵ����ԈD��(F)ͨ�^�ɹ��@�R�z����̥ROS���ɡ�
�C�ϣ����о����ýY���������������Ͱ��R�~ģ�ͣ��ɹ��ذlչ��һ�N�܉�ּ������Ѿ��Ұ������� hIAPP ���ۘӵ������ɵIJ��ԣ�ͬ�rҲ�lչ��һ�Nᘌ�hIAPP�ۼ��ĸ�Ч���Ƅ�����2�������A���c�ί����о���R�����Ý��������о��������Ե��ۘӵ��׳��e����c�������Լ���Ҳ�ṩ��һ�Nȫ�µ��ί��c�A��˼·��
�����о��ɹ��ڡ�ACS Nano���ھ��l�����}�顰Hierarchical Vitalization of Oligotyrosine in Mitigating Islet Amyloid Polypeptide Amyloidogenesis through Multivalent Macromolecules with Conformation-Restrained Nanobody Ligands�����A�пƼ���W��ʿ������������ʢ��������Փ�Ĺ�ͬ��һ���ߣ��A�пƼ���W�_���������Ϸ��ḱ������Փ�Ĺ�ͬͨӍ���ߡ�ԓ�о��õ��ˇ�����Ȼ�ƌW���𡢇��һ��A�о�Ӌ��������ʡ��Ȼ�ƌW����������У�������ИI���M��헻�����Y����
Փ��朽ӣ�https://doi.org/10.1021/acsnano.1c03083
- ���������W���i���ڈF� JACS����-�����錧�ĵ���ճ�� 2023-08-03
- �Ϻ��Ƽ���W犳��n�}�M��Sci. Adv.�����_�l�����ܿɾ��̵��ۘӵ���Ϳ�Ӳ��� 2020-05-21
- ���������i�����n�}�M�����ڵ����|��ۘӾۼ��Ŀ���Ϳ�� 2020-05-06
- �����A����ǻ�t�WԺ��ѩ�������n�}�M CEJ: �����{�����߷������پ����w�D�Ƶ�����ˮ���z���M�������Ԃ������� 2025-05-21
- ���ݴ�W���Ӱ��о��T�F� AFM��һ�N�������������Ե���λ���u���V�V�������r�ЙC���ˮ���z���ڴ��M���������� 2025-05-06
- ���_��W��������ڈF� JACS������ˮ���z�����f�������w - ����������ˎ����Ⱦ���������y�} 2025-05-06
