�錍�F�[���ľ����\�����_�l�[���h����TME���̼�푑��Գ����\���ˎ���f�͵����ܼ{��ˎ�����P��Ҫ��Ȼ���������[����λ���s�������Ͳ����ϵK�����F�{��ˎ��ĸ�Ч�[���f����Ȼ���R����������ˣ����_�l���������\���{��ƽ�_�r����Ҫ���]��N�ϵK����Ҫ��������������W���Ƥϵ�y��RES������Ĝ���Ч�������g�|Һ������Ѫ�ܝB©���ܰ����������ȡ����˿˷����ߺ�RES������������ڰ�����Ĥ��CCM���ϴ�������Ƭ�Ρ���ԭ��Ĥ�^���ף���NCCM�����ķ����{��ƽ�_���x�����������ݺ�ͬԴ�[���������������ˌ��F���ʵij����\�ࡢ��Ч���[���oˎ�ͽ���ȫ���������ã��OӋTME������pH���^�������ģ�GSH���ȣ��̼�푑���ጷ�ˎ������ܼ{��ˎ���Ȟ��P�I��
���ڼ{��ˎ����_�l���f�����y�ϳɷ��������T��ȱ�ݣ����؏����Ƃ���ͬ�������|��������ĸ��|���{��ƽ�_�����@���������ġ��e�Dz�ͬ���εļ{��ƽ�_��^���@������K�����R���D�����á����֮�£����ؼ��g�܉�ͨ�^���׳߶ȿ��g�ٿ����w�M�з��������Ծ��_���Ƽ{��ƽ�_�ĺϳ��^�̣������ɺˡ����L�;ۼ�����������һ�N����ǰ;�ļ��g������ԇ���p�ĵ͡��ɿ��Ƃ��һ���ϳɵ����c���ںϳɸ��|���{��ƽ�_��������ஔ�ă��ݣ��ܘO�������{��ˎ����R���D����
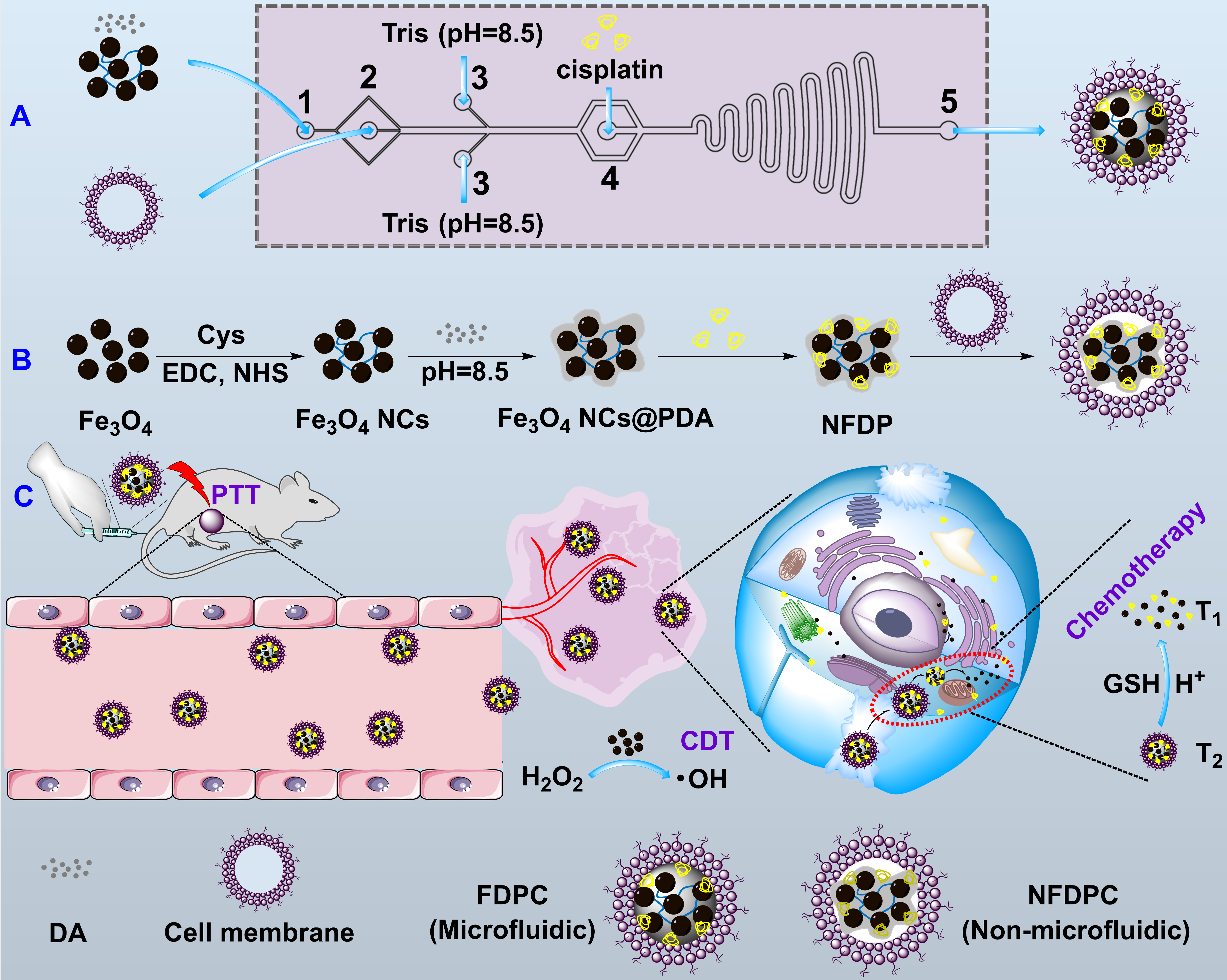
�D1. FDPC�������Ƃ䣨A����NFDPC�ķ������Ƃ䣨B���������ڄӑBT2/T1 MR���������[�����-���W-���W�����W��ģ�B���ί���ʾ��D��C����

�D2. ��ͬ����̎���ļ��������z�y�Y����A������ͬ��ʽ̎����������GSHˮƽ׃����r��B������C-D����ͬ��ʽ̎����������ROSˮƽ׃����r��

�D4. С���w���ί��^��ʾ��D��A�����ί�14���С���[���w�e���w��׃��������B-C�����ί���14���[����Ƭ��D�����ί���14���[����Ƭ��HE��TUNELȾɫ�Y����E�����ί���14����Ҫ�K����Ƭ��HEȾɫ�Y����F����
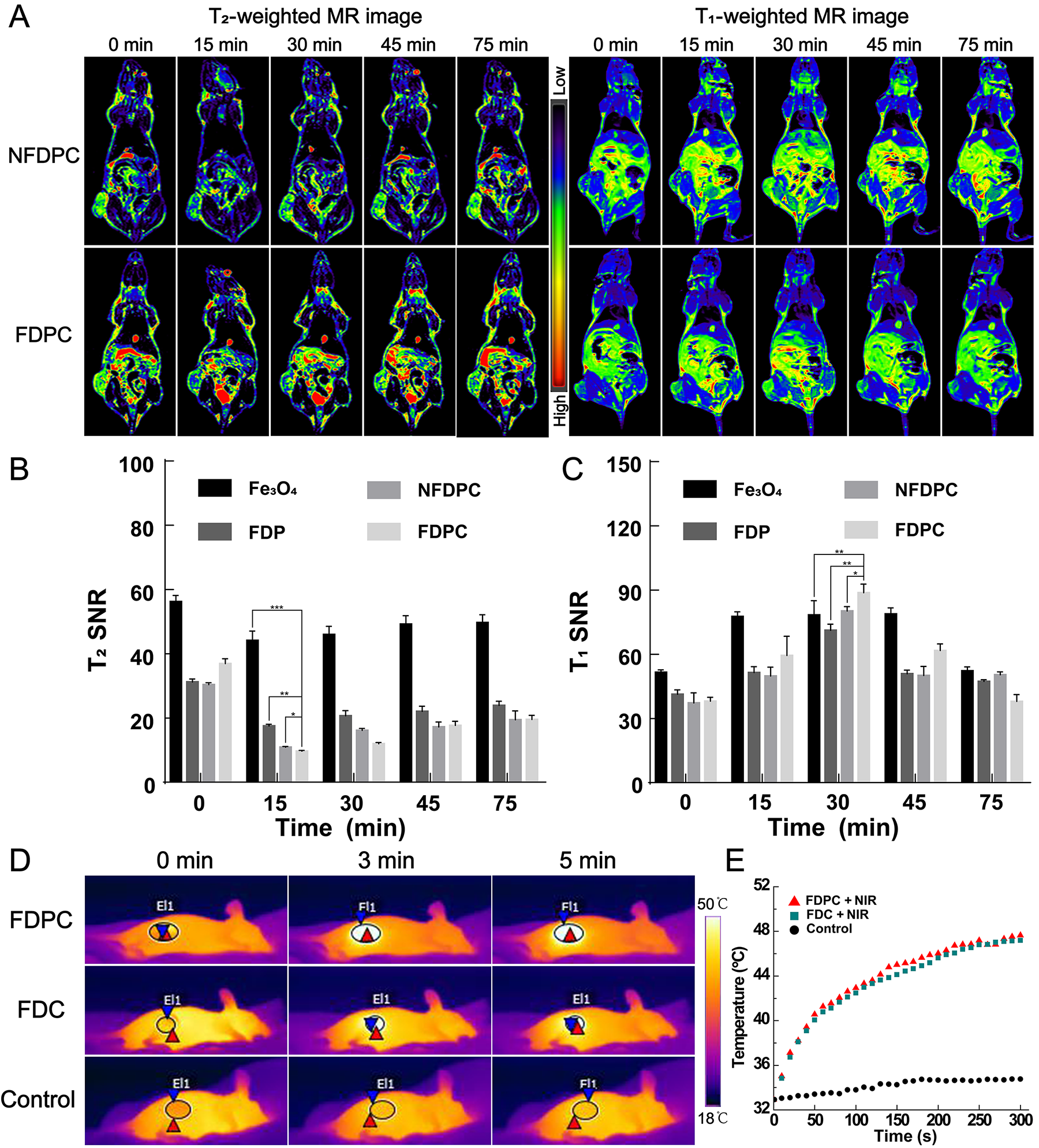
����֮��ԓ�о��OӋ��FDPC�{��ƽ�_����Ҫ�����������ׂ����棺1���c���y�W�����Ƃ���������ȣ��������صķ����Ƃ��FDPC�{��ƽ�_���и��õľ�һ�ԡ��z�w�����Ժ�TME�̼�ˎ��ጷ�������2��ͨ�^�����I�Ĕ�������GSH�ͻ��ڳ�С�F�錧��ROS���ɣ��{���[���h�������Ͱ������Ŀ�������������ʹ��������ˎ���ROS���У��p�ٶ���������3��FDPC�{��ƽ�_�������õ�ͬԴ�������ܡ�������ܺ�GSH푑���MR�������ܣ������ڰ����[��GSH푑��ĄӑBT2/T1 MR���������ί���
Փ��朽ӣ�https://doi.org/10.1016/j.nantod.2022.101615
- ���ϴ�W�Y���ס���������� CEJ��ͻ������оƬģ���I�ϼ��g 2024-12-19
- �����t�WԺY. Shrike Zhang���ڈF� PNAS���]�hģ�K�����_����������оƬϵ�y 2024-11-15
- ��������Ǭ���ڵȡ�Biosens. Bioelectron.������ָ��ʽ����оƬ���ڽY�˲��Ŀ��ٶ����\�� 2021-09-27
- ���д����ڣ��w�� / �Ʊ��҈F� ACS Nano �����AIE�{���R�_ͻ���[������ - ���F���ʹ��\�� 2025-05-29
- ɽ�|��W����ϼ���ڈF� Nat. Nanotech.���l�F��QCAR-T�����������w����Ч������Ч���� 2025-05-20
- ����ꐌW˼Ժʿ���O�o���ڈF� JACS��������o�����Ӿ����{���ܹ��������{���w�Sԭλ�ӑB�M�b���F�fͬ�[����Ч�ί� 2025-05-13
- �п�Ժ�ɶ���������ͽ��о��T�n�}�M���p���[���h���̼�푑��Լ{���fˎ�wϵ�о��@�Mչ 2017-11-27
